题目内容
14.下表各组物质中,物质之间不可能实现如图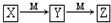 所示转化的是( )
所示转化的是( )| 选项 | X | Y | Z | M |
| A | Fe(s) | FeCl2 | FeCl3 | Cl2 |
| B | NaOH(aq) | Na2CO3 | NaHCO3 | CO2 |
| C | NH3(g) | NO | NO2 | O2 |
| D | S(s) | SO2 | SO3 | O2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Fe与氯气直接反应生成FeCl3;
B.NaOH与少量二氧化碳反应生成碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠;
C.氨气与氧气反应生成NO,NO与氧气反应生成二氧化氮;
D.硫和氧气反应生成二氧化硫,二氧化硫和氧气催化氧化生成三氧化硫.
解答 解:A.Fe与氯气反应不能生成FeCl2,不符合图中转化,故A选;
B.NaOH与少量二氧化碳反应生成碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠,符合图中转化,故B不选;
C.氨气与氧气反应生成NO,NO与氧气反应生成二氧化氮,符合图中转化,故C不选;
D.硫和氧气反应生成二氧化硫,二氧化硫和氧气催化氧化生成三氧化硫,可以实现,故D不选;
故选A.
点评 本题考查无机物的推断,侧重物质转化及物质性质的考查,明确常见物质的化学性质为解答的关键,注意选项A中氯气具有强氧化性,题目难度不大.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
4.欲制取较纯净的 1,2-二氯乙烷,可采用的方法是( )
| A. | 乙烯和 HCl 加成 | |
| B. | 乙烯和氯气加成 | |
| C. | 乙烷和 Cl2按 1:2 的体积比在光照条件下反应 | |
| D. | 乙烯先与 HCl 加成,再与等物质的量的氯气在光照条件下反应 |
5.已知常温下在溶液中可发生如下两个离子反应:
Ce 4++Fe 2+═Fe 3++Ce 3+
Sn 2++2Fe 3+═2Fe 2++Sn 4+
由此可以确定Fe 2+、Ce 3+、Sn 2+三种离子的还原性由强到弱的顺序是( )
Ce 4++Fe 2+═Fe 3++Ce 3+
Sn 2++2Fe 3+═2Fe 2++Sn 4+
由此可以确定Fe 2+、Ce 3+、Sn 2+三种离子的还原性由强到弱的顺序是( )
| A. | Sn 2+、Fe 2+、Ce 3+ | B. | Sn 2+、Ce 3+、Fe 2+ | ||
| C. | Ce 3+、Fe 2+、Sn 2+ | D. | Fe 2+、Sn 2+、Ce 3+ |
2.下列离子方程式不正确的是( )
| A. | 向Na2FeO4溶液中加入稀硫酸产生氧气:4FeO42-+20H+═4Fe3++3O2↑+10H2O | |
| B. | 10mL0.5mol/L的明矾溶液与20mL0.5mol/LBa(OH)2溶液混合反应:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ | |
| C. | 铜粉与63%的硝酸反应:Cu+4H++2NO3-═Cu2++2 NO2↑+2H2O | |
| D. | 工业上用纯碱液吸收SO2:CO32-+SO2═CO2+SO32- |
19.A、B为短周期元素,二者能形成化合物AB2,已知A的原子序数为n,则关于B的原子序数:①n+2 ②n+5 ③n+10 ④n+13 ⑤n-3 ⑥n-6 ⑦n-8 ⑧n+1,正确的是( )
| A. | ①②⑤可能 | B. | ④⑥不可能 | C. | ⑤⑥不可能 | D. | 都可能 |
2.草酸作为一种很重要的化工原料,某一个学习小组的同学拟用甘蔗渣为原料用水解一氧化一水解的技术来制取草酸如图1
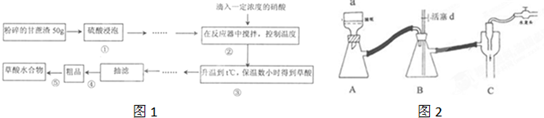
Ⅰ、步骤④是减压抽滤(如图2),其优点是:加快过滤速度、得到较干燥的沉淀,当抽滤完毕或中途停止抽滤时,为了防止自来水倒吸入B装置,最佳的操作是慢慢打开活塞d,然后关闭水龙头.
Ⅱ、该小组同学为了确定产品H2C2O4•xH2O中的x值,进行下列实验:
①取w g产品配成100mL水溶液;
②量取25.00mL草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol•L-1KMnO4溶液滴定. 请回答下列问题:
(1)实验①中,需要用到的玻璃仪器有:玻璃棒、烧杯、胶头滴管和100mL容量瓶.
(2)写出草酸溶液与酸性高锰酸钾溶液反应的离子方程式:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O.
(3)若滴定时,前后两次读数分别为a mL和b mL,由此计算出该草酸晶体的x值是$\frac{50W}{9c(b-a)}$-5
Ⅲ、该小组同学在做实验Ⅱ②时发现向草酸溶液中逐滴加入高锰酸钾溶液时,溶液褪色总是先慢后快,即反应速率由小变大.为此,他们设计了实验进行探究:
【实验用品】:仪器:试管(若干个并编号①,②,③…)、胶头滴管(若干支)、秒表
试剂:0.1mol/L H2C2O4溶液、0.1mol/L KMnO4溶液、稀硫酸、MnSO4固体
【实验内容】:实验(1):在①号和②号试管中分别先加入5m1 0.1mol/L H2C2O4溶液,然后各加10滴稀硫酸,且在②号试管中加入少量硫酸锰固体.再在两支试管中各加入5滴0.1mol/LKMnO4溶液.现象如下(表1)
实验(2):在①号和②号试管中分别加入5m1 0.1mol/L H2C2O4溶液,在②号试管中再滴加l0滴稀硫酸,然后在两支试管中各加入5滴0.1mol/L 的高锰酸钾溶液.现象如下(表2)
实验(3):在①号、②号和③号试管中分别加入5m1 0.1mol/L H2C2O4溶液,然后在①、②、③号试管中依次加入10滴、l mL、2mL稀硫酸溶液,然后各加入5滴0.1mol/L的高锰酸钾溶液,然后置于温度为65℃的水浴中加热.观察现象如下(表3).
(1)设计实验(1)对应的假设是反应产物中的Mn2+可能是反应的催化剂.
实验(1)得出的结论是Mn2+(或硫酸锰)在反应中起到催化剂的作用,加快了反应速率[或需要Mn2+(硫酸锰)作催化剂],假设1成立.
(2)由实验(2)和实验(3)得出的结论是由表2和表3的实验结果可知:硫酸对草酸和高锰酸钾溶液的反应有影响,加入少量硫酸,可促进草酸和KMnO4溶液反应,而加入大量硫酸,草酸和高锰酸钾溶液的反应速率开始比较慢,随着反应的进行,褪色速率加快,温度对该反应速率影响不大.

Ⅰ、步骤④是减压抽滤(如图2),其优点是:加快过滤速度、得到较干燥的沉淀,当抽滤完毕或中途停止抽滤时,为了防止自来水倒吸入B装置,最佳的操作是慢慢打开活塞d,然后关闭水龙头.
Ⅱ、该小组同学为了确定产品H2C2O4•xH2O中的x值,进行下列实验:
①取w g产品配成100mL水溶液;
②量取25.00mL草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol•L-1KMnO4溶液滴定. 请回答下列问题:
(1)实验①中,需要用到的玻璃仪器有:玻璃棒、烧杯、胶头滴管和100mL容量瓶.
(2)写出草酸溶液与酸性高锰酸钾溶液反应的离子方程式:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O.
(3)若滴定时,前后两次读数分别为a mL和b mL,由此计算出该草酸晶体的x值是$\frac{50W}{9c(b-a)}$-5
Ⅲ、该小组同学在做实验Ⅱ②时发现向草酸溶液中逐滴加入高锰酸钾溶液时,溶液褪色总是先慢后快,即反应速率由小变大.为此,他们设计了实验进行探究:
【实验用品】:仪器:试管(若干个并编号①,②,③…)、胶头滴管(若干支)、秒表
试剂:0.1mol/L H2C2O4溶液、0.1mol/L KMnO4溶液、稀硫酸、MnSO4固体
【实验内容】:实验(1):在①号和②号试管中分别先加入5m1 0.1mol/L H2C2O4溶液,然后各加10滴稀硫酸,且在②号试管中加入少量硫酸锰固体.再在两支试管中各加入5滴0.1mol/LKMnO4溶液.现象如下(表1)
| 编号 | ①号试管 | ②号试管 |
| 褪色时间 | 90s | 5s |
| 实验现象 | 均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色. | |
| 编号 | ①号试管 | ②号试管 |
| 褪色时间 | 100s | 90s |
| 实验现象 | 均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色. | |
| 编号 | ①号试管 | ②号试管 | ③号试管 |
| 褪色时间 | 88s | 100s | 120s |
| 实验现象 | 均有气泡产生;①号试管的溶液褪色比②、③号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色. | ||
实验(1)得出的结论是Mn2+(或硫酸锰)在反应中起到催化剂的作用,加快了反应速率[或需要Mn2+(硫酸锰)作催化剂],假设1成立.
(2)由实验(2)和实验(3)得出的结论是由表2和表3的实验结果可知:硫酸对草酸和高锰酸钾溶液的反应有影响,加入少量硫酸,可促进草酸和KMnO4溶液反应,而加入大量硫酸,草酸和高锰酸钾溶液的反应速率开始比较慢,随着反应的进行,褪色速率加快,温度对该反应速率影响不大.
20.下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
| 甲 | 乙 | 丙 | |
| A | Na | H2O | Cl2 |
| B | Al | Fe2O3 | 稀H2SO4 |
| C | CH3CH2OH | NaOH溶液 | CH3COOH |
| D | Ba(OH)2溶液 | CO2 | Na2CO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白: