题目内容
将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应:2A(气) + B(气)  2C(气)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1 ② 用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1 ③2 s 时物质 B 的浓度为 0.7 mol·L-1 ④2 s 时物质 A 的转化率为70% 其中正确的是( )
2C(气)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1 ② 用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1 ③2 s 时物质 B 的浓度为 0.7 mol·L-1 ④2 s 时物质 A 的转化率为70% 其中正确的是( )
A.①③ B.①④ C.②③ D.③④
 口算题天天练系列答案
口算题天天练系列答案SO2随意排放会造成严重的大气污染。下列是某小组同学设计处理烟气(主要含SO2、N2、O2、粉尘)中SO2的方法。
(1)方法一:利用氯碱工业产品处理SO2的烟气,流程如下:

①“吸收装置”中发生反应的离子方程式_____________________。
②合成塔中每合成1mol气体放出热量92.3kJ(25℃、101kPa),反应的热化学方程式_____________。
③上述流程中循环利用的物质是____________________。
(2)方法二:利用FeCl3溶液氧化吸收烟气中SO2
①该反应的离子方程式________________________(反应a)。为验证该反应,同学们将SO2通入0.05mol/LFeCl3溶液中,溶液很快由 黄色变为红褐色;将溶液长时间放置后,最终变
黄色变为红褐色;将溶液长时间放置后,最终变 为浅绿色。关于红褐色液体,以下是同学们的分析推测
为浅绿色。关于红褐色液体,以下是同学们的分析推测 与
与 实验。
实验。
分析推测 | 实验步骤及现象 |
甲:生成了Fe(OH)3胶体 乙: Fe3++6SO2 | I、制备Fe(OH)3胶体并检验 II、分别向Fe(OH)3胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 |
②利用胶体的_________________(填性质)可以检验步骤I中是否得到了Fe(OH)3胶体。
③根据反应b说明步骤II中液体颜色变化的原因是______________________(用离子方程式及必要的文字说明)。


 CO(g)+H2(g) △H=+131.3kJ/mol
CO(g)+H2(g) △H=+131.3kJ/mol 中的C(s)部分移走,平衡将 (填序号)。
中的C(s)部分移走,平衡将 (填序号)。
 CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
 染,常采用氢氧化钠溶液进行吸收处理。反应方程式:2NO2 + 2NaOH=NaNO3 + NaNO2 + H2O;NO2 + NO + 2NaOH=2NaNO2+H2O 现有由a mol NO、b m
染,常采用氢氧化钠溶液进行吸收处理。反应方程式:2NO2 + 2NaOH=NaNO3 + NaNO2 + H2O;NO2 + NO + 2NaOH=2NaNO2+H2O 现有由a mol NO、b m ol NO2、c mol N2O4组成的混合气体恰好被V L氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度为( ) mol/L
ol NO2、c mol N2O4组成的混合气体恰好被V L氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度为( ) mol/L B.
B.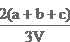 C.
C.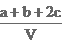 D.
D.
 经查阅资料,可能发生反应:
经查阅资料,可能发生反应: Fe(SO2)63+(反应b)
Fe(SO2)63+(反应b)