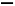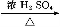题目内容
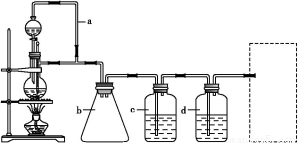
A、B、C、D、E均为有机化合物,转化关系如图所示:
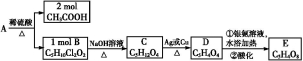
已知:一个碳原子上连有两个羟基时,其结构极不稳定,易发生下列变化,生成较稳定物质:
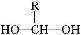
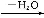
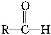
请回答下列问题:
(1)化合物A的分子式: 。
(2)B的结构简式: 。
(3)写出A→B,C→D的有机反应类型:A→B: 反应,C→D: 反应。
(4)B不能发生的反应是 (填序号)。
①氧化反应;②取代反应;③消去反应;④水解反应;⑤加聚反应
(5)写出D与足量的银氨溶液在一定条件下反应的化学方程式: 。
(1)C9H14Cl2O4 (2)(ClCH2)2C(CH2OH)2
(3)取代(或水解) 氧化 (4)③⑤
(5)C(CHO)4+8Ag(NH3)2OH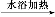 C(COONH4)4+8Ag↓+12NH3+4H2O
C(COONH4)4+8Ag↓+12NH3+4H2O
【解析】根据题目给定信息由E→D→C逆向推导可知C的结构简式为C(CH2OH)4,则B的结构简式为(ClCH2)2C(CH2OH)2,D为C(CHO)4,E为C(COOH)4,A为(ClCH2)2C(CH2OOCCH3)2,故A的分子式为C9H14Cl2O4。

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目