题目内容
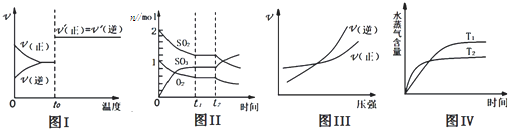
反应2SO2+O2?2SO3在一定温度下达到平衡,下列说法正确的是( )
分析:A.增大压强平衡向气体体积减小的方向移动,平衡常数只受温度影响,与压强无关;
B.二氧化硫与氧气按2:1反应,二者起始浓度为2:1时平衡时浓度满足c(SO2)=2c(O2);
C.增大某一反应物的浓度,平衡向正反应方向移动,其它反应物的转化率增大;
D.根据改变的可能条件进行分析解答.
B.二氧化硫与氧气按2:1反应,二者起始浓度为2:1时平衡时浓度满足c(SO2)=2c(O2);
C.增大某一反应物的浓度,平衡向正反应方向移动,其它反应物的转化率增大;
D.根据改变的可能条件进行分析解答.
解答:解:A.正反应为气体体积减小的反应,增大压强平衡向正反应方向移动,平衡常数只受温度影响,压强不变,故A错误;
B.二氧化硫与氧气按2:1反应,二者起始浓度为2:1时平衡时浓度满足c(SO2)=2c(O2),但二者起始浓度不一定是2:1,故平衡时二者浓度不一定满足c(SO2)=2c(O2),故B错误;
C.增大氧气的浓度,平衡向正反应方向移动,二氧化硫的转化率增大,故C正确;
D.若增大二氧化硫的浓度,平衡向正反应方向移动,平衡时三氧化硫的浓度增大、二氧化硫的浓度也增大,氧气的浓度减小,若增大压强平衡向正反应方向移动,反应混合物的浓度都增大,故D错误,
故选C.
B.二氧化硫与氧气按2:1反应,二者起始浓度为2:1时平衡时浓度满足c(SO2)=2c(O2),但二者起始浓度不一定是2:1,故平衡时二者浓度不一定满足c(SO2)=2c(O2),故B错误;
C.增大氧气的浓度,平衡向正反应方向移动,二氧化硫的转化率增大,故C正确;
D.若增大二氧化硫的浓度,平衡向正反应方向移动,平衡时三氧化硫的浓度增大、二氧化硫的浓度也增大,氧气的浓度减小,若增大压强平衡向正反应方向移动,反应混合物的浓度都增大,故D错误,
故选C.
点评:本题考查化学平衡的影响因素,难度中等,D选项为易错点,可以借助平衡常数理解浓度、压强改变引起平衡移动时平衡时各浓度的变化.

练习册系列答案
相关题目
反应2SO2+O2?2SO3,5s内SO3的浓度增加了0.4mol/L,则在这段时间内用O2表示的反应速率(mol/L?s)为( )
| A、0.1 | B、0.08 | C、0.04 | D、0.02 |
 ( )
( )