题目内容
【题目】红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(图中的ΔH表示生成1 mol产物的数据)。
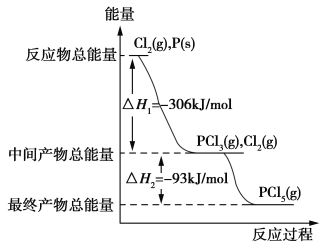
根据图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式为_____________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式为_____________________。
(3)P和Cl2分两步反应生成1 mol PCl5的ΔH3=________,P和Cl2一步反应生成1 mol PCl5的ΔH4________(填“>”“<”或“=”)ΔH3。
【答案】P(s)+![]() Cl2(g)=PCl3(g) ΔH=-306 kJ/mol PCl5(g)=Cl2(g)+PCl3(g) ΔH=+93 kJ/mol -399kJ/mol =
Cl2(g)=PCl3(g) ΔH=-306 kJ/mol PCl5(g)=Cl2(g)+PCl3(g) ΔH=+93 kJ/mol -399kJ/mol =
【解析】
(1)根据图象,生成气态的PCl3,ΔH =-306 kJ/mol。P为固体,Cl2 为气体,则热化学方程式为P(s)+![]() Cl2(g)=PCl3(g) ΔH=-306 kJ/mol;
Cl2(g)=PCl3(g) ΔH=-306 kJ/mol;
答案为:P(s)+![]() Cl2(g)=PCl3(g) ΔH=-306 kJ/mol (2)从图象来看, PCl3(g)和Cl2 (g)生成PCl5 (g),ΔH =- 93 kJ/mol。现在要求PCl5 (g)分解成PCl3(g)和Cl2(g),ΔH应为+ 93 kJ/mol。则热化学方程式为PCl5(g)=Cl2(g)+PCl3(g) ΔH=+93 kJ/mol ;
Cl2(g)=PCl3(g) ΔH=-306 kJ/mol (2)从图象来看, PCl3(g)和Cl2 (g)生成PCl5 (g),ΔH =- 93 kJ/mol。现在要求PCl5 (g)分解成PCl3(g)和Cl2(g),ΔH应为+ 93 kJ/mol。则热化学方程式为PCl5(g)=Cl2(g)+PCl3(g) ΔH=+93 kJ/mol ;
答案为:PCl5(g)=Cl2(g)+PCl3(g) ΔH=+93 kJ/mol (3)从图象来看,ΔH3=ΔH1+ΔH2=- 306 kJ/mol+ ( -93 kJ/mol)= -399 kJ/mol。化学反应热△H只和反应物、生成物的能量有关,与反应路径无关,只要反应物和生成物一样,不管是经过一步还是二步反应,反应热相同,因此ΔH4等于ΔH3。
答案为:-399 kJ/mol ;=

【题目】某学习小组对SO2使溶液褪色的机理进行探究。
I.SO2气体的制备和性质初探
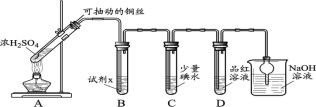
(1)装置A中发生反应的化学方程式____________。
(2)装置B中的试剂x是____________。
(3)小组同学观察到C、D中溶液均褪色,通过检验C溶液中有SO42-,得出C中溶液褪色的原因是____________。
II.小组同学通过实验继续对D中品红溶液褪色进行探究。
(4)探究使品红褪色的主要主要微粒(分别取2 mL试剂a,滴加2滴品红溶液)
装置 | 序号 | 试剂a | 实验现象 |
| i | 0.1 mol/L SO2溶液(pH=2) | 红色逐渐变浅,之后完全褪色 |
ii | 0.1 mol/L NaHSO3溶液(pH=5 ) | 红色立即变浅,之后完全褪色 | |
iii | 0.1 mol/L Na2SO3溶液( pH=10) | 红色立即褪色 | |
iv | pH=2H2SO4溶液 | 红色无明显变化 | |
v | 试剂a | 红色无明显变化 |
①实验 iii中Na2SO3溶液显碱性的原因_____________(结合化学用语分析解释)。
②对比实验iii 和v,可以排除在该实验条件下OH-对品红褪色的影响,则试剂a可能
是__________溶液。
查阅资料:品红与SO2水溶液、NaHSO3溶液、Na2SO3溶液反应前后物质如下:
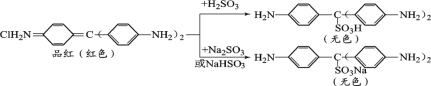
③通过上述实验探究并结合资料,小组同学得出结论:一是使品红溶液褪色的主要微粒是________;二是品红溶液中颜色变化主要与其分子中的________结构有关。
(5)验证SO2使品红褪色反应的可逆性
①甲同学加热实验i褪色后的溶液,产生刺激性气味气体,红色恢复,从化学平衡移动角度解释红色恢复的原因__________。
②乙同学向实验i褪色后的溶液中滴入Ba(OH)2溶液至pH=10,生成白色沉淀,溶液变红。写出生成白色沉淀的离子方程式___________。
③丙同学利用SO2的还原性,运用本题所用试剂,设计了如下实验,证实了SO2使品红褪色反应的可逆:则试剂Y是__________。