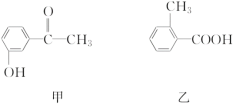
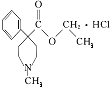
题目内容
【题目】已知:X、Y、Z、M、N、A 均为中学化学中的常见物质。(部分生成物及条件略去)
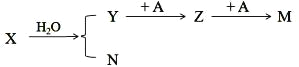
(1)若 X 为红棕色气体,A 为日常生活中应用最广泛的金属,写出 X 与 H2O 反应的化学方程式: __,Z 为_________(写化学式);
(2)若 X 为淡黄色固体,M 为难溶于水的物质,且 X 与 M 具有相同的摩尔质量,则 X 的电子式 _______,A 中参加反应简单阳离子的结构示意图为_________________ ;若 1mol X 与水反应经上述转化,能得到 M 的最大质量__
(3)若 M、N 为同一物质,且为厨房中某常用调味品主要成分。写出 Y 与 N 反应生成 X 的反应类型:_____,检验 Y 中是否混有 M 的简便实验方法___________________________________ .向盛少量 KMnO4 溶液的试管中先滴入少量硫酸,再滴加 Y,充分振荡红色褪去,并生成 M。写出发生反应的离子方程式__________________________________.
【答案】3NO2+H2O=2HNO3+NO Fe(NO3)3 ![]()
![]() 52g 酯化反应/取代反应 取少量混合物于试管中,加适量水再滴加几滴紫色石蕊溶液,若溶液变红,则乙醇中混有乙 酸 , 反 之 则 不 含 乙 酸 5CH3CH2OH+4MnO4-+12H+→5CH3COOH+4Mn2++11H2O
52g 酯化反应/取代反应 取少量混合物于试管中,加适量水再滴加几滴紫色石蕊溶液,若溶液变红,则乙醇中混有乙 酸 , 反 之 则 不 含 乙 酸 5CH3CH2OH+4MnO4-+12H+→5CH3COOH+4Mn2++11H2O
【解析】
(1)红棕色气体可以是NO2或Br2,但后续反应中Br2不能全部进行。日常生活中应用最广泛的金属为铁。铁和硝酸反应生成硝酸铁,硝酸铁和铁生成硝酸亚铁。
(2)淡黄色固体常见的有S、Na2O2、AgBr,能和水反应的只有Na2O2。M 为难溶于水的物质,且 X 与 M 具有相同的摩尔质量,则M为氢氧化铝。A 为硫酸铝氯化铝等铝盐溶液。
(3)厨房中常用调味品考虑NaCl、CH3COOH,由于M、N 为同一物质,Y 能使酸性KMnO4 溶液褪色,则M、N为CH3COOH,Y 为乙醇,Z 为乙醛,X 为乙酸乙酯。
(1)由图中信息可知,X 为 NO2,A 为金属铁,Z 为硝酸铁,M 为硝酸亚铁,X 与 H2O 反应的化学方程式:3NO2+H2O=2HNO3+NO;答案为:3NO2+H2O=2HNO3+NO; Fe(NO3)3。
(2)结合图示和题目信息可知 X 为过氧化钠,A 为铝盐溶液,M 为氢氧化铝,所以 X 的电子式为:![]() ,A 中简单阳离子即铝离子的结构示意图为
,A 中简单阳离子即铝离子的结构示意图为![]() ;1mol 过氧化钠与水反应生成氢氧化钠 2mol,故最多可得氢氧化铝 2/3mol,即 52g;答案为:
;1mol 过氧化钠与水反应生成氢氧化钠 2mol,故最多可得氢氧化铝 2/3mol,即 52g;答案为:![]() ;
; ![]() ;52g。
;52g。
(3)由题给信息可知,该反应是乙酸乙酯的水解,Y 为乙醇,Z 为乙醛,M 为乙酸。乙醇与乙酸反应生成酯为酯化反应/取代反应。检验醇中混酸,可取少量混合物于试管中,加适量水再滴加几滴紫色石蕊溶液,若溶液变红,则乙醇中混有乙酸,反之则不含乙酸;硫酸酸化的高锰酸钾溶液与乙醇反应的离 子 方 程 式 :5CH3CH2OH+4MnO4-+12H+→5CH3COOH+4Mn2++11H2O。答案为:酯化反应/取代反应 ; 取少量混合物于试管中,加适量水再滴加几滴紫色石蕊溶液,若溶液变红,则乙醇中混有乙 酸 , 反 之 则 不 含 乙 酸 ;5CH3CH2OH+4MnO4-+12H+→5CH3COOH+4Mn2++11H2O。

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案【题目】用下图表示的一些物质或概念间的从属关系中,不正确的是( )
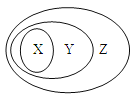
X | Y | Z | |
例 | 氧化物 | 化合物 | 纯净物 |
A | 苯的同系物 | 芳香烃 | 芳香族化合物 |
B | 烯烃 | 不饱和烃 | 烃 |
C | 减压蒸馏 | 常压蒸馏 | 石油的分馏 |
D | 油脂的皂化 | 酯的水解 | 取代反应 |
A. A B. B C. C D. D