题目内容
16.A由Al2O3、Fe3O4、Al、Cu中的某几种粉末混合而成,该混合物成分的分析方案如图所示.下列分析错误的是( )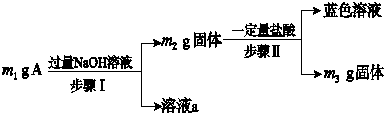
| A. | 当m1>m2时,溶液a中的阴离子只有1种 | |
| B. | 生成蓝色溶液的离子方程式为Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 要确定混合物中是否含有Al,可取A加入适量稀盐酸 | |
| D. | 当m2-m3=2.96 g时,Fe3O4的质量至少为2.32 g |
分析 A.当m1>m2时,说明至少有Al2O3、Al两者中的一种,且生成了偏铝酸钠溶液;
B.Fe3O4与盐酸反应生成氯化铁和氯化亚铁,三价铁离子有强氧化性;
C.金属氧化物与酸反应生成水,无氢气,而铜与盐酸不反应;
D.引固体质量改变的金属氧化物的溶解,和三价铁与铜单质之间的氧化还原反应.
解答 解:A.铝、氧化铝都能和氢氧化钠反应,Fe3O4、Cu和氢氧化钠不反应,当m1>m2时,说明至少有Al2O3、Al两者中的一种,且生成了偏铝酸钠溶液,而过量的氢氧化钠,阴离子大于一种,故A错误;
B.Fe3O4与盐酸反应生成氯化铁和氯化亚铁,三价铁离子有强氧化性,发生Cu+2Fe3+═Cu2++2Fe2+,故B正确;
C.金属氧化物与酸反应生成水,无氢气,而铜与盐酸不反应,可取A加入适量稀HCl,如果有气体产生,证明铝的存在,故C正确;
D.固体质量改变的原因有:金属氧化物的溶解,三价铁与铜单质之间的氧化还原反应,Cu+2Fe3+=Cu2++2Fe2+,Fe3O4~2Fe3+~Cu,也就是四氧化三铁和铜的物质的量大于1:1,m2-m3=2.96g才符合,最小值为1:1,即2.96g×$\frac{232}{232+64}$×100%=2.32 g,故D正确;
故选A.
点评 本题考查常见金属元素及化合物的综合应用,题目难度中等,要通过实验现象得出结论,再结合定量计算得出结论.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2 L二氯甲烷( CH2Cl2)所含的分子数为0.5NA | |
| B. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA | |
| C. | 1mol羟基(-OH)所含的电子总数为10NA | |
| D. | 10g质量分数为46%的乙醇溶液中,氢原子的总数为1.2NA |
7.重金属是指相对原子质量大于55的金属,重金属离子具有毒性.实验室有甲、乙两种含重金属离子的废液,甲废液经化验呈碱性,主要有毒离子为Ba2+.如将甲、乙废液按一定比例混合,毒性明显降低.则乙废液中可能会有的离子是( )
| A. | Cu2+和SO42- | B. | K+和SO42- | C. | Cu2+和Cl- | D. | Ag+和NO3- |
4.实验室需用480mL0.10mol/L的硫酸铜溶液,以下操作正确的是( )
| A. | 将12.00g胆矾配成500mL溶液 | |
| B. | 将12.50g胆矾溶于少量水中,再用水稀释至500mL | |
| C. | 称取7.68g硫酸铜,加入500mL水 | |
| D. | 在80mL0.6mol/L CuSO4溶液中加入400mL水 |
11.能够证明苯分子不存在碳碳单、双键交替排布的事实是( )
| A. | 苯的一溴代物没有同分异构体 | B. | 苯的间位二溴代物只有一种 | ||
| C. | 苯能在空气中燃烧 | D. | 苯的邻位二溴代物只有一种 |
8.向一体积不变的密闭容器中加入2mol A、0.6mol C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图1所示.图2为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件.
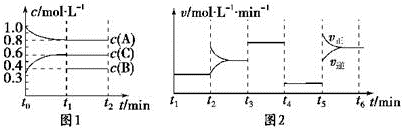
已知t3-t4阶段为使用催化剂;图1中t0-t1阶段c (B)未画出.
(1)若t1=15min,则t0-t1阶段以C浓度变化表示的反应速率为v(C)=0.02mol•L-1•min-1.
(2)(2)t4-t5阶段改变的条件为减小压强,B的起始物质的量为1.0mol.各阶段平衡时对应的平衡常如表所示:
则K1=0.84(保留两位小数),K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5(用“>”“<”或“=”连接).
(3)t5-t6阶段保持容器内温度不变,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为a kJ,写出此温度下该反应的热化学方程式:2A(g)+B(g)?3C(g);△H=+200a kJ•mol-1.
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,达到平衡时体系中各物质的量与t1时刻相等,a、b、c要满足的条件为a+$\frac{2}{3}$c=2.4且b+$\frac{1}{3}$c=1.2.

已知t3-t4阶段为使用催化剂;图1中t0-t1阶段c (B)未画出.
(1)若t1=15min,则t0-t1阶段以C浓度变化表示的反应速率为v(C)=0.02mol•L-1•min-1.
(2)(2)t4-t5阶段改变的条件为减小压强,B的起始物质的量为1.0mol.各阶段平衡时对应的平衡常如表所示:
| t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
| K1 | K2 | K3 | K4 | K5 |
(3)t5-t6阶段保持容器内温度不变,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为a kJ,写出此温度下该反应的热化学方程式:2A(g)+B(g)?3C(g);△H=+200a kJ•mol-1.
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,达到平衡时体系中各物质的量与t1时刻相等,a、b、c要满足的条件为a+$\frac{2}{3}$c=2.4且b+$\frac{1}{3}$c=1.2.
5. 天然气、可燃冰的主要成分都是甲烷,甲烷既是一种清洁能源,又是一种重要的化工原料.
天然气、可燃冰的主要成分都是甲烷,甲烷既是一种清洁能源,又是一种重要的化工原料.
(1)以甲烷为主要原料可以生成合成气(CO和H2),主要反应如下:有研究认为甲烷部分氧化的机理为:
①CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-802.3kJ•mol-1
②CO(g)+H2O(g)═H2(g)+CO2(g);△H=-41.2kJ•mol-1
③2CO(g)+O2(g)═2CO2(g);△H=-566.0kJ•mol-1
则反应CH4(g)+CO2(g)═2CO(g)+2H2(g)的△H=+247.3kJ/mol.
(2)CH4也可以和H2O(g)在催化剂表面反应生成合成气:CH4(g)+H2O(g)═3H2(g)+CO(g),该反应在不同温度下的化学平衡常数K如下表:
(1)该反应△H>0(选填“>”或“<”);
(2)已知800℃时,向1L密闭容器中投入0.5molCH4、0.5mol H2O、0.5molH2和0.5molCO,则平衡时向正向移动(选填“正向移动”、“逆向移动”或“不移动”.
(3)工业上利用合成气在恒容、催化剂和加热的条件下可以生产甲醇,其热化学方程式为:2H2(g)+CO(g)═CH3OH(g)△H=-90.8kJ/mol.
①以下各项能说明该反应达到平衡状态的是AB.
A、混合气体的平均式量保持不变
B、混合气体的压强不变
C、混合气体的密度保持不变
D、2v逆(H2)=v正(CH3OH)
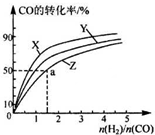
②在200℃、230℃和260℃三种不同温度、2L恒容密闭容器中研究合成甲醇的规律,如图是上述三种温度下不同的H2和C0的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,则曲线Z对应的温度是260℃.由起始达到 a 点所需时间为 5min,则 H2的反应速率 为0.1mol/(L•min).
(4)以熔融Li2CO3和K2CO3为电解质,向一极通入甲烷,另一极通入空气和CO2,甲烷可形成燃料电池.负极的电极反应式为CH4-8e-+4CO32-=5CO2+2H2O,若该装置的电流强度为1.6A,理论上每分钟应向负极通入标准状况下的气体约为2.8mL.(已知:一个电子所带电量为1.6×10-19C)
 天然气、可燃冰的主要成分都是甲烷,甲烷既是一种清洁能源,又是一种重要的化工原料.
天然气、可燃冰的主要成分都是甲烷,甲烷既是一种清洁能源,又是一种重要的化工原料.(1)以甲烷为主要原料可以生成合成气(CO和H2),主要反应如下:有研究认为甲烷部分氧化的机理为:
①CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-802.3kJ•mol-1
②CO(g)+H2O(g)═H2(g)+CO2(g);△H=-41.2kJ•mol-1
③2CO(g)+O2(g)═2CO2(g);△H=-566.0kJ•mol-1
则反应CH4(g)+CO2(g)═2CO(g)+2H2(g)的△H=+247.3kJ/mol.
(2)CH4也可以和H2O(g)在催化剂表面反应生成合成气:CH4(g)+H2O(g)═3H2(g)+CO(g),该反应在不同温度下的化学平衡常数K如下表:
| 温度(℃) | 800 | 1000 | 1200 | 1400 |
| 平衡常数(K) | 0.45 | 1.92 | 276.5 | 1771.5 |
(2)已知800℃时,向1L密闭容器中投入0.5molCH4、0.5mol H2O、0.5molH2和0.5molCO,则平衡时向正向移动(选填“正向移动”、“逆向移动”或“不移动”.
(3)工业上利用合成气在恒容、催化剂和加热的条件下可以生产甲醇,其热化学方程式为:2H2(g)+CO(g)═CH3OH(g)△H=-90.8kJ/mol.
①以下各项能说明该反应达到平衡状态的是AB.
A、混合气体的平均式量保持不变
B、混合气体的压强不变
C、混合气体的密度保持不变
D、2v逆(H2)=v正(CH3OH)
②在200℃、230℃和260℃三种不同温度、2L恒容密闭容器中研究合成甲醇的规律,如图是上述三种温度下不同的H2和C0的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,则曲线Z对应的温度是260℃.由起始达到 a 点所需时间为 5min,则 H2的反应速率 为0.1mol/(L•min).
(4)以熔融Li2CO3和K2CO3为电解质,向一极通入甲烷,另一极通入空气和CO2,甲烷可形成燃料电池.负极的电极反应式为CH4-8e-+4CO32-=5CO2+2H2O,若该装置的电流强度为1.6A,理论上每分钟应向负极通入标准状况下的气体约为2.8mL.(已知:一个电子所带电量为1.6×10-19C)