题目内容
12.氰氨化钙(CaCN2)是一种碱性肥料,也是高效低毒农药的主要原料之一.(1)Ca、C、N三种元素的第一电离能由小到大的顺序为Ca、C、N.
(2)基态Ca2+的核外电子排布式为1s22s22p63s23p6.
(3)若CN22-的中心C原子为sp杂化,则CN22-中σ键和π键的个数比1:1.
分析 (1)元素的非金属性越强,其第一电离能越大;
(2)Ca为20号元素,有4个电子层,最外层电子数为2,失去最外层的2个电子后形成Ca2+,据此解答即可;
(3)CN22-的中心C原子为sp杂化,得到2个电子达到最外层8个电子的稳定结构,据此解答即可.
解答 解:(1)由于非金属性N>C>Ca,故第一电离能Ca<C<N,故答案为:Ca、C、N;
(2)Ca为20号元素,有4个电子层,最外层电子数为2,失去最外层的2个电子后形成Ca2+,其核外电子排布式为:1s22s22p63s23p6,故答案为:1s22s22p63s23p6;
(3)CN22-的中心C原子为sp杂化,得到2个电子后,C与N均达到最外层8个电子的稳定结构,即C与N形成三键,N与N形成单键,含有的σ键和π键的个数比为2:2=1:1,故答案为:1:1.
点评 本题主要考查的是第一电离能的大小比较、离子核外电子层排布、化学键的判断等,综合性较强,难度一般.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
2.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.请回答下列问题:
(1)上述实验中发生反应的离子方程式有Zn+Cu2+=Zn2++Cu、Zn+2H+=Zn2++H2↑;
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应中,收集产生的气体,记录获得相同体积的气体所需时间.
①请完成此实验设计,其中:V1=30,V6=10,V9=17.5;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降,请分析氢气生成速率下降的主要原因当加入一定量的硫酸铜后,生成的单质铜会沉积在Zn表面,降低了Zn与溶液接触的表面,使得氢气的生成速率反而下降;
(3)改用锌粉与稀硫酸反应,加入少量硫酸铜溶液后充分振荡,一段时间剩余少量固体.该同学对固体成分提出下列假设:
假设1:全部为铜;
假设2:既有Zn又有Cu.
(4)请你设计实验验证上述假设1,完成下表内容.
(1)上述实验中发生反应的离子方程式有Zn+Cu2+=Zn2++Cu、Zn+2H+=Zn2++H2↑;
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应中,收集产生的气体,记录获得相同体积的气体所需时间.
| 实验 | A | B | C | D | E | F | |
| 混 合 溶 液 | 4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 | |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 | |
| 时间(min) | 15 | 10 | 5 | 3 | 6 | 9 | |
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降,请分析氢气生成速率下降的主要原因当加入一定量的硫酸铜后,生成的单质铜会沉积在Zn表面,降低了Zn与溶液接触的表面,使得氢气的生成速率反而下降;
(3)改用锌粉与稀硫酸反应,加入少量硫酸铜溶液后充分振荡,一段时间剩余少量固体.该同学对固体成分提出下列假设:
假设1:全部为铜;
假设2:既有Zn又有Cu.
(4)请你设计实验验证上述假设1,完成下表内容.
| 实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
| , |
3.离子液体是一种室温熔融盐,为非水体系,由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体作电解液时,可在钢制品上电镀铝.下列电解原理正确的是( )
| A. | 钢制品应接电源的正极 | |
| B. | 电镀时铝作阳极,阳极反应式为Al-3e-+7AlCl4-=4Al2Cl7- | |
| C. | 电解液中H+移向阴极,OH-移向阳极 | |
| D. | 每生成1mol铝,电解液中转移3mol电子 |
7.用惰性电极电解CuSO4溶液一段时间,停止后,向所得溶液中加入0.2molCu(OH)2,恰好使溶液恢复至电解前,关于电解过程说法不正确的是( )
| A. | 生成的铜的物质的量是0.2mol | B. | 随着电解进行溶液的pH减小 | ||
| C. | 转移电子的物质的量为0.4mol | D. | 阳极反应是2H2O-4e-=4H++O2↑ |
17.乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中错误的是( )
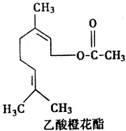

| A. | 分子式为C12H20O2 | |
| B. | 能使酸性KMnO4溶液褪色 | |
| C. | 能发生加成反应,但不能发生取代反应 | |
| D. | 1mol该有机物水解时只能消耗lmolNaOH |
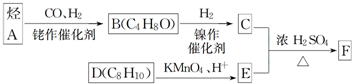
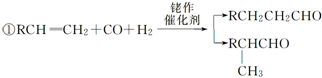
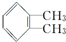 ,名称为邻二甲苯.
,名称为邻二甲苯.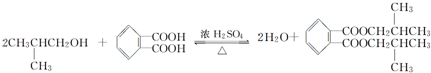 .
. ;X分子中有2种不同化学环境的氢原子,其峰面积之比为1:2;1mol X与NaOH溶液共热反应,最多消耗4 mol NaOH.
;X分子中有2种不同化学环境的氢原子,其峰面积之比为1:2;1mol X与NaOH溶液共热反应,最多消耗4 mol NaOH.
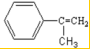

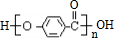
 ;反应⑦n
;反应⑦n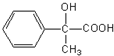 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$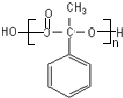 +(n-1)H2O
+(n-1)H2O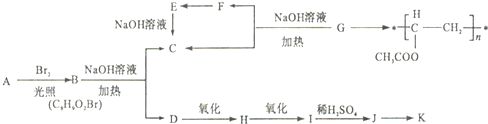
 .
. .
.