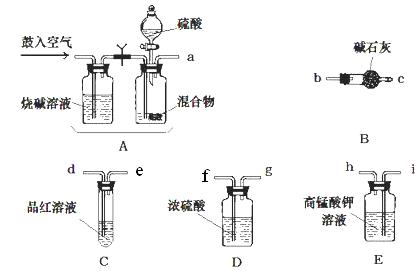
题目内容
某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
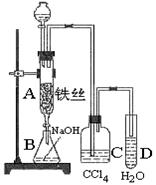
(1)写出A中反应的化学方程式:
(2)A中的现象是 。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关的化学方程式 。
(4)C中盛放CCl4的作用是 。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入 ,现象是

(1)写出A中反应的化学方程式:
(2)A中的现象是 。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关的化学方程式 。
(4)C中盛放CCl4的作用是 。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入 ,现象是
(本题共12分)(1)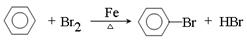
(2)反应液微沸有红棕色气体充满A容器
(3)除去溶于溴苯中的溴 Br2 + 2NaOH NaBr + NaBrO + H2O
NaBr + NaBrO + H2O
或2Br2 + 6NaOH 5NaBr + NaBrO3 + 3H2O
5NaBr + NaBrO3 + 3H2O
(4)除去溴化氢气体中的溴蒸气 (5)石蕊试液,溶液变红色 (其他合理答案都给分)

(2)反应液微沸有红棕色气体充满A容器
(3)除去溶于溴苯中的溴 Br2 + 2NaOH
 NaBr + NaBrO + H2O
NaBr + NaBrO + H2O或2Br2 + 6NaOH
 5NaBr + NaBrO3 + 3H2O
5NaBr + NaBrO3 + 3H2O(4)除去溴化氢气体中的溴蒸气 (5)石蕊试液,溶液变红色 (其他合理答案都给分)
试题分析:(1)A装置是制取溴苯的,则A中反应的化学方程式
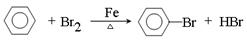 。
。(2)由于反应是放热反应,且溴易挥发,所以Z装置中的实验现象是反应液微沸,有红棕色气体充满A容器。
(3)由于生成的溴苯中含有单质溴,所以实验的目的是除去溶于溴苯中的溴,有关反应的方程式是Br2 + 2NaOH
 NaBr + NaBrO + H2O或2Br2 + 6NaOH
NaBr + NaBrO + H2O或2Br2 + 6NaOH 5NaBr + NaBrO3 + 3H2O。
5NaBr + NaBrO3 + 3H2O。(4)由于生成溴化氢中含有单质溴,会干扰溴化氢的检验,所以四氯化碳的作用是除去溴化氢气体中的溴蒸气。
(5)由于溴化氢溶于水,溶液显酸性,所以还可以利用石蕊试液检验,实验现象是溶液变红色。
点评:该题是高考中的常见题型,属于中等难度的试题,试题基础性强,难易适中。在注重对基础知识巩固和训练的同时,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生规范严谨的实验设计能力以及评价能力。该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。

练习册系列答案
相关题目
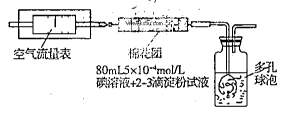
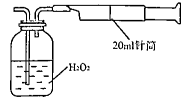 所示简易装置进行实验。实验操作如下:按图安装好仪器,在广口瓶中盛放足量的H2O2水溶液,用规格为20mL的针筒抽气100次,使空气中的SO2被H2O2水溶液充分吸收(SO2+H2O2=H2SO4)。在吸收后的水溶液中加入足量的BaCl2溶液,生成白色沉淀,经过滤、洗涤、干燥等步骤后进行称量,得白色固体0.182mg。
所示简易装置进行实验。实验操作如下:按图安装好仪器,在广口瓶中盛放足量的H2O2水溶液,用规格为20mL的针筒抽气100次,使空气中的SO2被H2O2水溶液充分吸收(SO2+H2O2=H2SO4)。在吸收后的水溶液中加入足量的BaCl2溶液,生成白色沉淀,经过滤、洗涤、干燥等步骤后进行称量,得白色固体0.182mg。
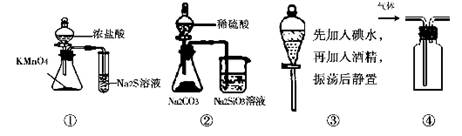
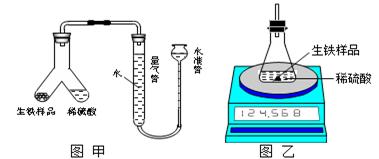
 H2S + 2OH –
H2S + 2OH – 。回答以下问题:
。回答以下问题: