题目内容
19.下列溶液一定显碱性的是( )| A. | c(OH-)>c(H+)的溶液 | |
| B. | 含OH-的溶液 | |
| C. | pH=3的CH3COOH与pH=11的NaOH溶液等体积混合 | |
| D. | 滴加甲基橙后溶液显红色 |
分析 A.一种溶液显酸性、中性还是碱性,取决于溶液中c(H+)和c(OH-)的相对大小;
B、水溶液中一定含有水的电离,溶液这一定含氢氧根离子和氢离子;
C、醋酸是弱酸溶液中存在电离平衡,随反应进行又电离出氢离子,溶液显酸性;
D、甲基橙指示剂的变色范围为3.1-4.4,算溶液中显示红色.
解答 解:A、碱性溶液:c(H+)<c(OH-),c(OH-)越大,碱性越强,故A正确;
B、水溶液中一定含有水的电离,溶液这一定含氢氧根离子和氢离子,不一定显碱性,如氯化钠溶液是中性溶液,故B错误;
C、pH=3的CH3COOH与pH=11的NaOH溶液等体积混合,醋酸溶液中氢离子浓度和氢氧化钠溶液中氢氧根离子浓度相同,等体积混合,醋酸是弱酸溶液中存在电离平衡,随反应进行又电离出氢离子,溶液显酸性,故C错误;
D、甲基橙指示剂的变色范围为3.1-4.4,算溶液中显示红色,碱性溶液可以显黄色,故D错误;
故选A.
点评 本题考查溶液的酸碱性和指示剂变色范围,难度不大,平时注意知识的积累,掌握基础是关键.

练习册系列答案
相关题目
7.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 6.0gSiO2晶体中含有0.2NA个Si-O键 | |
| B. | 1L1mol•L-1CH3COOH溶液中,所含CH3COO-、CH3COOH的总数为NA | |
| C. | 1L1mol•L-1饱和FeCl3溶液滴入沸水中完全水解生成Fe(OH)3胶体粒子数为NA个 | |
| D. | 10g46%的乙醇水溶液中所含H原子数为0.6NA |
4.下列各组物质中,两者互为同分异构体的是( )
| A. | 2CaSO4•H2O和CaSO4•2H2O | B. | CH3CH2OH与CH3OCH3 | ||
| C. | CuSO4•3H2O与CuSO4•5H2O | D. | H2O与D2O(重水) |
9.在反应:11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,15molCuSO4可氧化磷原子的物质的量为( )
| A. | $\frac{1}{5}$mol | B. | 2mol | C. | 3 mol | D. | 6mol |
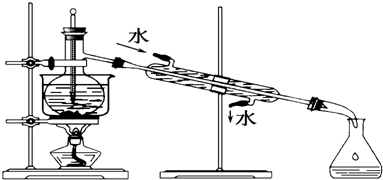
 丙炔腈(H-C=C-CN,沸点42.5℃)是一种星际分子,实验室可通过丙炔醇用铬酸酐氧化、盐酸羟胺肟化、再脱水来制备.
丙炔腈(H-C=C-CN,沸点42.5℃)是一种星际分子,实验室可通过丙炔醇用铬酸酐氧化、盐酸羟胺肟化、再脱水来制备.