��Ŀ����
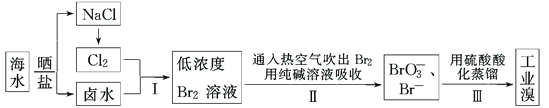
����Ŀ������ʵ�����Ʒ�����������ε����ʽ���̽����
�ش��������⣺
�������Ʊ�
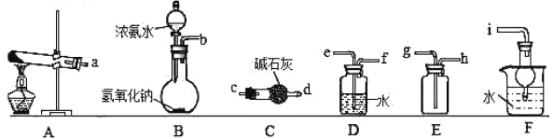
��1������Aװ���Ʊ�������д����Ӧ�Ļ�ѧ����ʽ_______________�����ռ�һƿ����İ�����ѡ����ͼ�е�װ�ã����ظ�ʹ�ã���������˳��Ϊ��a��___________��������������Сд��ĸ��ʾ����
��2����װ��B����Ũ��ˮ���������ƹ����ϣ�Ҳ���Ƶð���������÷����Ʊ�������ԭ ��________________________��
����ͼװ�ý��а���������ʵ�飨����1������2ʵ��ǰ�رգ���G��H�������������������
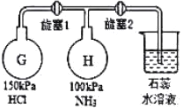
��3���ȴ�����I��Hƿ��������________________��ԭ����________________��һ��ʱ��ر�����1���ٴ������2��Hƿ��������_________��
�����ʵ�飬̽��ijһ���ض�һ�����ʵ���Ũ��NH4Clˮ��̶ȵ�Ӱ�졣
��ѡ�Լ���������NH4Cl���塢����ˮ���ձ�����ͷ�ιܡ���������ҩ�ס�������ƽ��pH�ơ��¶ȼơ�����ˮԡ�ۣ��ɿ����¶ȣ�
��4����������������ȱ��һ����Ҫ�IJ�����������������_______________��
��5�����������������Լ����������Ʋ�ʵ��Ŀ�ģ�̽��_______��NH4Clˮ��̶ȵ�Ӱ�졣
���𰸡� 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O a��c��d��h��g����d��c��c��d����i ��֪��ˮ�д��ڣ�
CaCl2+2NH3��+2H2O a��c��d��h��g����d��c��c��d����i ��֪��ˮ�д��ڣ� ![]() ��������������ˮ����ˮ���Ĺ����Ƿ��ȵģ���ʹNH3��H2O�ֽ�ų����� ��ˮ���������ƻ�Ϻ�����������������Һ�е����������ӵ�Ũ�ȣ�ʹ��ˮ�е�ƽ�����ƣ������ڰ����ݳ� �а��̣��������Ȼ�粒��� ʯ����Һ������Hƿ�У�ʯ����Һ����˺�ɫ ����ƿ Ũ�Ȼ����¶�
��������������ˮ����ˮ���Ĺ����Ƿ��ȵģ���ʹNH3��H2O�ֽ�ų����� ��ˮ���������ƻ�Ϻ�����������������Һ�е����������ӵ�Ũ�ȣ�ʹ��ˮ�е�ƽ�����ƣ������ڰ����ݳ� �а��̣��������Ȼ�粒��� ʯ����Һ������Hƿ�У�ʯ����Һ����˺�ɫ ����ƿ Ũ�Ȼ����¶�
�����������������(1)Aװ���ʺϼ��ȹ�����ȡ���壬������ȡ�������Ȼ�狀��������ƣ��Ʊ�����İ������ü�ʯ�Ҹ�����������ſ������ռ��ռ������β��������(2)����ƽ���ƶ�ԭ���� (3)G��ѹǿ����H��������1 ���Ȼ������H���백����Ӧ�����Ȼ�泥������������ɹ��壬G��H�е�ѹǿ��С��������2 ��ʯ�����H��(4)����ʵ��Ŀ��̽��ijһ���ض�һ�����ʵ���Ũ��NH4Clˮ��̶ȵ�Ӱ�죬��Ҫ����һ�����ʵ���Ũ�ȵ��Ȼ����Һ��(5)�����ṩ�������¶ȼơ�����ˮԡ�۷���ʵ��Ŀ�ġ�
������(1)��Aװ����ȡ�������Ȼ�狀��������ƣ�����ʽΪ2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O���Ʊ�����İ������ü�ʯ�Ҹ�����������ſ������ռ��ռ������β����������������˳��Ϊa��c��d��h��g����d��c��c��d����i ��(2)����ƽ���ƶ�ԭ������ˮ�д��ڣ�
CaCl2+2NH3��+2H2O���Ʊ�����İ������ü�ʯ�Ҹ�����������ſ������ռ��ռ������β����������������˳��Ϊa��c��d��h��g����d��c��c��d����i ��(2)����ƽ���ƶ�ԭ������ˮ�д��ڣ�![]() ��������������ˮ����ˮ���Ĺ����Ƿ��ȵģ���ʹNH3��H2O�ֽ�ų��������������������ƻ�Ϻ�����������������Һ�е����������ӵ�Ũ�ȣ�ʹ��ˮ�е�ƽ�����ƣ������ڰ����ݳ������Կ���B��ȡ������ (3)G��ѹǿ����H��������1 ���Ȼ������H���백����Ӧ�����Ȼ�泥�H���а��̣��������Ȼ�粒��壻�����������ɹ��壬G��H�е�ѹǿ��С��������2 ��ʯ����Һ������Hƿ�У������Ȼ����Һ�����ԣ�ʯ����Һ����˺�ɫ��(4)����ʵ��Ŀ��̽��ijһ���ض�һ�����ʵ���Ũ��NH4Clˮ��̶ȵ�Ӱ�죬������Ҫ����һ�����ʵ���Ũ�ȵ��Ȼ����Һ��ȱ������ƿ��(5)�����ṩ�������¶ȼơ�����ˮԡ�۷���ʵ��Ŀ����Ũ�Ȼ����¶ȶ�һ�����ʵ���Ũ��NH4Clˮ��̶ȵ�Ӱ�졣
��������������ˮ����ˮ���Ĺ����Ƿ��ȵģ���ʹNH3��H2O�ֽ�ų��������������������ƻ�Ϻ�����������������Һ�е����������ӵ�Ũ�ȣ�ʹ��ˮ�е�ƽ�����ƣ������ڰ����ݳ������Կ���B��ȡ������ (3)G��ѹǿ����H��������1 ���Ȼ������H���백����Ӧ�����Ȼ�泥�H���а��̣��������Ȼ�粒��壻�����������ɹ��壬G��H�е�ѹǿ��С��������2 ��ʯ����Һ������Hƿ�У������Ȼ����Һ�����ԣ�ʯ����Һ����˺�ɫ��(4)����ʵ��Ŀ��̽��ijһ���ض�һ�����ʵ���Ũ��NH4Clˮ��̶ȵ�Ӱ�죬������Ҫ����һ�����ʵ���Ũ�ȵ��Ȼ����Һ��ȱ������ƿ��(5)�����ṩ�������¶ȼơ�����ˮԡ�۷���ʵ��Ŀ����Ũ�Ȼ����¶ȶ�һ�����ʵ���Ũ��NH4Clˮ��̶ȵ�Ӱ�졣

 �������ϵ�д�
�������ϵ�д�����Ŀ����Ԫ�صĻ������ж��֡�
�ش��������⣺
��1��SiH4�ķе��CH4�ߣ�ԭ����____________________________________��
��2������̼ͬ���壬Ҳ��ϵ���⻯�������������������϶�Զ���������ࡣ�����±��� ���м������ݣ���Ҫ�������ܵ�ԭ��___________________________________��
��ѧ�� | C��C | C��H | Si��Si | Si��H |
����/(kJ��mol-1) | 356 | 413 | 226 | 318 |
�����裨Si3N4����һ����Ҫ���մɲ��ϣ�����ʯӢ�뽹̿��800��ĵ��������ºϳɣ�
3SiO2(s)+6C(s)+2N2(g) ![]() Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
��3�����������Ӧ�е���ת�Ƶ���Ŀ�ͷ���____________��
��4���÷�Ӧ��ƽ�ⳣ������ʽK=____________����֪ƽ�ⳣ����K(800��)>K(850��)����Ӧ��_________��Ӧ������ȡ������ȡ�����
��5����д��������߶�������ת���ʵĴ�ʩ_________________��_________________��
��6��һ���¶��£���2L�ܱ������ڣ�����һ�����ķ�Ӧ�5����ʱ�ﵽƽ�⣬�������������������0.4mol����CO��ʾ�÷�Ӧʱ���ڵķ�Ӧ����Ϊ_________________��