题目内容
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO等氧化物)制取金属锌的流程如图所示。回答下列问题:

(1)酸浸时ZnFe2O4会生成两种盐,该反应的化学方程式为___________。
(2)净化Ⅰ操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,使Fe3+转化为Fe(OH)3沉淀。
①写出酸性条件下H2O2与Fe2+反应的离子方程式:___________。
②25 ℃时,pH=3的溶液中,c(Fe3+)=________mol·L-1(已知25 ℃,Ksp[Fe( OH)3]=4.0×10-38)。
③净化Ⅰ生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是____________________。
(3)若没有净化Ⅱ操作,则对锌的制备带来的影响是_________________。
⑷本流程中可以循环利用的物质除锌外还有________________。

(1)酸浸时ZnFe2O4会生成两种盐,该反应的化学方程式为___________。
(2)净化Ⅰ操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,使Fe3+转化为Fe(OH)3沉淀。
①写出酸性条件下H2O2与Fe2+反应的离子方程式:___________。
②25 ℃时,pH=3的溶液中,c(Fe3+)=________mol·L-1(已知25 ℃,Ksp[Fe( OH)3]=4.0×10-38)。
③净化Ⅰ生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是____________________。
(3)若没有净化Ⅱ操作,则对锌的制备带来的影响是_________________。
⑷本流程中可以循环利用的物质除锌外还有________________。
(13分,第(1)小题3分,其余每空2分)
(1)ZnFe2O4+4H2SO4=ZnSO4+Fe2(SO4)3+4H2O
(2)①H2O2+2Fe2++2H+=2Fe3++2H2O;②4.0×10-5;③Fe(OH)3胶体(沉淀)具有吸附性;(3)制取的锌含铜等杂质;(4)H2SO4、ZnSO4 (每空2分,共12分)
(1)ZnFe2O4+4H2SO4=ZnSO4+Fe2(SO4)3+4H2O
(2)①H2O2+2Fe2++2H+=2Fe3++2H2O;②4.0×10-5;③Fe(OH)3胶体(沉淀)具有吸附性;(3)制取的锌含铜等杂质;(4)H2SO4、ZnSO4 (每空2分,共12分)
(1)根据信息,酸浸时ZnFe2O4会生成两种盐,这两种盐分别为硫酸锌、硫酸铁,即ZnFe2O4与硫酸反应生成硫酸锌、硫酸铁,反应的化学方程式为:ZnFe2O4+4H2SO4═ZnSO4+Fe2(SO4)3 +4H2O,
答案为:ZnFe2O4+4H2SO4═ZnSO4+Fe2(SO4)3 +4H2O;
(2)①亚铁离子被双氧水氧化成铁离子,反应的离子方程式为H2O2+2Fe2++2H+═2Fe3++2H2O,答案为:H2O2+2Fe2++2H+═2Fe3++2H2O;
②氢氧化铁的溶度积Ksp[Fe(OH)3 ]=4.0×10-38,pH=3的溶液中,氢氧根离子的浓度为1×10-11mol·L-1,c(Fe3+)=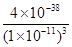 mol·L-1=4.0×10-5mol·L-1,
mol·L-1=4.0×10-5mol·L-1,
答案为:4.0×10-5;
③由于生成的Fe(OH)3胶体(沉淀)具有吸附性,所以净化Ⅰ生成的沉淀中还含有溶液中的悬浮杂质,答案为:Fe(OH)3胶体(沉淀)具有吸附性;
(3)由于锌焙砂中含有CaO、FeO、CuO、NiO等氧化物,反应后溶液中存在铜离子,没有净化Ⅱ操作,电解制取的锌中会含有铜等杂质,答案为:制取的锌含铜等杂质;
(4)通过制取金属锌的流程图示可以知道,可以循环利用的物质除锌外,含有硫酸、硫酸锌,
答案为:H2SO4、ZnSO4.
答案为:ZnFe2O4+4H2SO4═ZnSO4+Fe2(SO4)3 +4H2O;
(2)①亚铁离子被双氧水氧化成铁离子,反应的离子方程式为H2O2+2Fe2++2H+═2Fe3++2H2O,答案为:H2O2+2Fe2++2H+═2Fe3++2H2O;
②氢氧化铁的溶度积Ksp[Fe(OH)3 ]=4.0×10-38,pH=3的溶液中,氢氧根离子的浓度为1×10-11mol·L-1,c(Fe3+)=
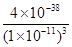 mol·L-1=4.0×10-5mol·L-1,
mol·L-1=4.0×10-5mol·L-1,答案为:4.0×10-5;
③由于生成的Fe(OH)3胶体(沉淀)具有吸附性,所以净化Ⅰ生成的沉淀中还含有溶液中的悬浮杂质,答案为:Fe(OH)3胶体(沉淀)具有吸附性;
(3)由于锌焙砂中含有CaO、FeO、CuO、NiO等氧化物,反应后溶液中存在铜离子,没有净化Ⅱ操作,电解制取的锌中会含有铜等杂质,答案为:制取的锌含铜等杂质;
(4)通过制取金属锌的流程图示可以知道,可以循环利用的物质除锌外,含有硫酸、硫酸锌,
答案为:H2SO4、ZnSO4.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目

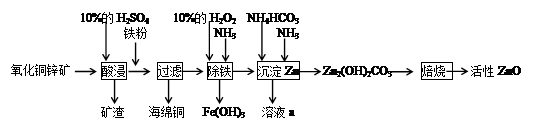
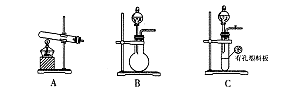
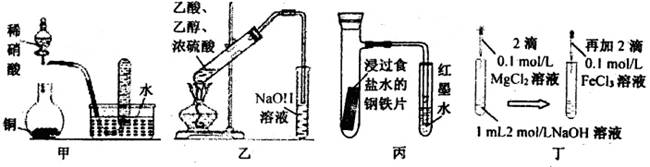
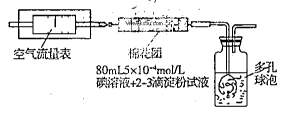
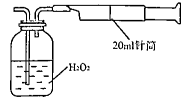 所示简易装置进行实验。实验操作如下:按图安装好仪器,在广口瓶中盛放足量的H2O2水溶液,用规格为20mL的针筒抽气100次,使空气中的SO2被H2O2水溶液充分吸收(SO2+H2O2=H2SO4)。在吸收后的水溶液中加入足量的BaCl2溶液,生成白色沉淀,经过滤、洗涤、干燥等步骤后进行称量,得白色固体0.182mg。
所示简易装置进行实验。实验操作如下:按图安装好仪器,在广口瓶中盛放足量的H2O2水溶液,用规格为20mL的针筒抽气100次,使空气中的SO2被H2O2水溶液充分吸收(SO2+H2O2=H2SO4)。在吸收后的水溶液中加入足量的BaCl2溶液,生成白色沉淀,经过滤、洗涤、干燥等步骤后进行称量,得白色固体0.182mg。