题目内容
【题目】下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料。
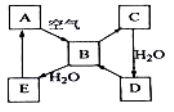
(1)写出A在加热条件下与H2反应的化学方程式________________
(2)写出E与A的氢化物反应生成A的化学方程式___________________________
(3)写出一个由D生成B的化学方程式___________________________;
(4)将5mL0.10mol·L-1的E溶液与10mL0.10 mol·L-1的NaOH溶液混合。写出反应的离子方程式________________;
【答案】
(1)H2+S![]() H2S(或写成可逆符号)
H2S(或写成可逆符号)
(2)H2SO3+2H2S=3S+3H2O
(3)C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O或Cu+2H2SO4(浓)
CO2↑+2SO2↑+2H2O或Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(4)H2SO3+2OH-=SO32-+ 2H2O
【解析】
试题分析:固态单质A能与空气中的氧气反应生成气体物质B,则A可能为C或S等,假定为S,则B为SO2,C为SO3,它们的相对分子质量为64:80=4:5,恰好与题意相符(同时也证明A不是C),则D为H2SO4,它是一种重要的工业原料,与题意也相符,进一步证明A为S,E为H2SO3,
(1)A为S,可与氢气反应生成硫化氢,反应的方程式为H2+S![]() H2S,故答案为:H2+S
H2S,故答案为:H2+S![]() H2S;
H2S;
(2)H2SO3与H2S反应生成S,反应的方程式为H2SO3+2H2S═3S↓+3H2O,故答案为:H2SO3+2H2S═3S↓+3H2O;
(3)浓硫酸可与C、Cu等还原性物质在加热的条件下反应生成SO2,反应的方程式可为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O或Cu+2H2SO4(浓)
CO2↑+2SO2↑+2H2O或Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O等,故答案为:C+2H2SO4(浓)
CuSO4+SO2↑+2H2O等,故答案为:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O或Cu+2H2SO4(浓)
CO2↑+2SO2↑+2H2O或Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O等;
CuSO4+SO2↑+2H2O等;
(4)将5mL 0.10molL-1的H2SO3溶液与10mL 0.10molL-1的NaOH溶液混合,二者恰好反应,反应的离子方程式为H2SO3+2OH-═SO32-+2H2O,故答案为:H2SO3+2OH-═SO32-+2H2O。

 阅读快车系列答案
阅读快车系列答案
