题目内容
【题目】已知1mol白磷变成1mol红磷放出18.39kJ的热量。下列两个方程式:
4P(白磷,s)+ 5O2(g)= 2P2O5(s);△H1
4P(红磷,s)+ 5O2(g)= 2P2O5(s);△H2
则△H1和△H2的关系正确的是
A.△H1 = △H2 B.△H1 > △H2 C.△H1 < △H2 D.不能确定
【答案】C
【解析】
试题分析:①4P(白)+5O2═2P2O5 △H1;②4P(红)+5O2=2P2O5 △H2,①-②得到4P(白)=4P(红)△H=△H1-△H2,已知1mol白磷变成1mol红磷放出18.39KJ的热量,所以△H1-△H2<0;△H1<△H2,故选C。

练习册系列答案
相关题目
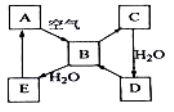
【题目】含A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物C可用于制造高性能的现代通讯材料—光导纤维,C与烧碱反应生成含A元素的化合物D
(1)B元素的原子最外层电子数与A相同,则B在元素周期中的位置___ __.
(2)写出易与C发生反应的酸与C反应的化学方程式是______________.
(3)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E:将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F.
①写出生成D的化学反应方程式:______________.
②要将纯碱高温熔化,下列坩埚中不可选用的是__________.
A.普通玻璃坩埚 | B.石英玻璃坩埚 | C.铁坩埚 | D.瓷坩埚. |
③将过量的E通入D的溶液中发生反应的离子方程式是:_________________。
(4)100 g C与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是____________。