题目内容
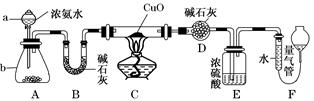
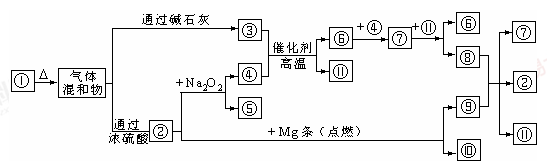
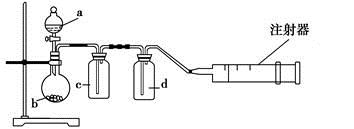
无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100 mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为


| A.NH3、NO2、N2(体积比5∶16∶4) |
| B.NH3、NO、CO2(体积比5∶8∶12) |
| C.NH3、NO2、CO2 (体积比3∶8∶4) |
| D.NO、CO2、N2(体积比8∶12∶5) |
B
试题分析:该无色气体通过足量的浓硫酸,时氨气被吸收,由于气体体积减小20ml,则氨气的体积为20ml;再通过足量的Na2O2的干燥管时,气体变为红棕色,则说明原气体中含有NO和CO2。发生反应:2Na2O2+2CO2 =Na2CO3+ O2;O2+2NO=2NO2。当气体通过足量的水时由于得到酸性溶液,而几乎无气体剩余。所以没有N2。发生反应:O2+4NO2+2H2O=4HNO3。或3O2+4NO+2H2O=4HNO3.由上述方程式得关系式为6CO2~3O2~4NO则在剩余的80ml的气体中CO2的体积为80ml×6/10=48ml;NO的体积为80ml×4/10=32ml。因此在原混合气体中含有NH3、NO、CO2。它们的物质的量的比或体积比为20:32:48=5∶8∶12。故选项为B。

练习册系列答案
相关题目
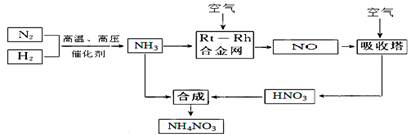
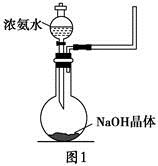

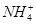 +OH-,NaOH晶体使该可逆反应的平衡向左移动
+OH-,NaOH晶体使该可逆反应的平衡向左移动