题目内容
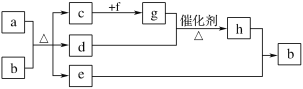
【题目】短周期元素W、X、Y、Z、Q的原子序数依次增大,c、d、e、f、h是由这些元素组成的二元化合物,自然界中硬度最大的单质和a都由X组成,b由W、Y、Q三种元素组成,d能使品红溶液褪色,e是液体,上述物质的转化关系如图所示(个别产物略去)。下列说法错误的是( )
A.二元化合物沸点:e>d>c
B.简单氢化物的稳定性:Q>Y>X
C.元素的非金属性:Y>X>W
D.原子半径的大小:Z>Q>Y
【答案】B
【解析】
自然界中硬度最大的单质和a都由X组成,则X应为C元素,a为木炭;d能使品红溶液褪色,则d应为SO2;e是液体,结合题给转化关系及b由W、Y、Q三种元素组成,可推出b为浓H2SO4,c为CO2,e为H2O;e和h反应生成b,结合e、b的化学式及h是二元化合物,可知h为SO3,d和g在催化剂、加热条件下生成h,则g为O2,c和f反应生成g,f是二元化合物,则f为Na2O2。综上所述,W、X、Y、Z、Q分别为H、C、O、Na、S。
A.水分子常温下为液态,CO2、SO2常温下为气体,其相对分子质量越大,沸点越高,故沸点由大到小的顺序为H2O>SO2>CO2,A选项正确;
B.元素非金属性越强,简单氢化物越稳定,非金属性:O>S>C,则简单氢化物的稳定性:H2O>H2S>CH4,B选项错误;
C.同周期主族元素从左到右非金属性逐渐增强,故非金属性:O>C,H的非金属性较弱,则非金属性:O>C>H,C选项正确;
D.同周期主族元素从左到右原子半径逐渐减小,同主族元素随原子核外电子层数增多,原子半径增大,则原子半径的大小关系为Na>S>O,D选项正确;
答案选B。

【题目】某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定,其实验装置如图所示.
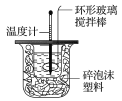
(1)写出该反应的热化学方程式(中和热为57.3 kJ·mol-1):___________________________________。
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。请填写下表中的空白:
温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | _____ |
2 | 27.0 | 27.4 | 27.2 | 31.2 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
(3)近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。则中和热ΔH=________________________(取小数点后一位)。
(4)上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是____________(填字母)。
a 实验装置保温、隔热效果差
b 量取NaOH溶液的体积时仰视读数
c 分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d 用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度