题目内容
【题目】在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法正确的是
A. 反应可表示为:X(g)+Y(g) ![]() 2Z(g)
2Z(g)
B. 反应达到平衡时,X的转化率为60%
C. 在此条件下,该反应的平衡常数为K=1600
D. 其他条件不变时,增大压强平衡发生移动,再达新平衡,平衡常数增大
【答案】C
【解析】A.由表中数据可知,达到平衡时,X、Y的浓度减小、Z的浓度增大,则X、Y为反应物、Z为生成物,根据反应物浓度变化量之比等于化学计量数之比可知:△c(X):△c(Y):△c(Z):=0.05:0.15:0.1=1:3:2,则反应的方程式为X+3Y![]() 2Z,故A错误;B.反应达到平衡时,X的转化率为:
2Z,故A错误;B.反应达到平衡时,X的转化率为: ![]() ×100%=50%,故B错误;C. 该反应的化学方程式为:X+3Y
×100%=50%,故B错误;C. 该反应的化学方程式为:X+3Y![]() 2Z,则K=
2Z,则K=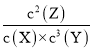 =
=![]() =1600,故C正确;D.平衡常数只与温度有关,增大压强平衡发生移动,但平衡常数不变,故D错误;答案选C。
=1600,故C正确;D.平衡常数只与温度有关,增大压强平衡发生移动,但平衡常数不变,故D错误;答案选C。

练习册系列答案
相关题目