��Ŀ����
����Ŀ�����ʼ�������26�λ��������˰����ӵ�����(NA=6.02214076��1023mol��1)������2019��5��20����ʽ��Ч������˵����ȷ����
A. 56g����ϩ�����к�̼̼˫������ĿΪ2 NA
B. 2 mol NH3��3molO2�ڴ����ͼ��������³�ַ�Ӧ����NO�ķ�����Ϊ2 NA
C. Ǧ���طŵ�ʱ����������������������������16gʱת�Ƶ�����ΪNA
D. 1L0.5mlol��L��1Al2Fe(SO4)4��Һ����������ĿС��1.5 NA
���𰸡�C
��������
A������ϩ�в���̼̼˫����ѡ��A����
B��4NH3+5O2![]() 4NO+6H2O���÷�ӦΪ���淴Ӧ���ʰ���������ȫת��ΪNO���ҹ�����O2������NO��Ӧ����NO2��ѡ��.B����
4NO+6H2O���÷�ӦΪ���淴Ӧ���ʰ���������ȫת��ΪNO���ҹ�����O2������NO��Ӧ����NO2��ѡ��.B����
C��Pb+ PbO2 +2H2SO4![]() 2PbSO4(s)+ 2H2O��ת��2 mol����ʱ������������96g��������������64 g������32g��ѡ��C��ȷ��
2PbSO4(s)+ 2H2O��ת��2 mol����ʱ������������96g��������������64 g������32g��ѡ��C��ȷ��
D��A13+��Fe2+ˮ�����H+�������Ӱ���H+���������������ӣ���1L0.5 mol/L Al2Fe(SO4)4��Һ����������Ŀ����1.5NA��ѡ��D�����
��ѡC��

 һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�����Ŀ�����Ĺ̶��Ǽ���������ѧ��һֱ�о��Ŀ��⡣��ش��������⣺
(1)�±��о��˲�ͬ�¶��´����̵���ҵ�̵��IJ���Kֵ��
��Ӧ | �����̵� N2 (g)+O2 (g) | ��ҵ�̵� N2 (g)+3H2 (g) | |||
�¶�/�� | 27 | 2000 | 25 | 400 | 450 |
K | 3.84��10��31 | 0.1 | 5��108 | 0.507 | 0.152 |
���������ݿ�֪�������̵���Ӧ���� ________(����ȡ����ȡ�)��Ӧ��
���������ݿ�֪������ʺϴ��ģģ������̵���ԭ���� ________��
�۴�ƽ���ӽǿ��ǣ���ҵ�̵�Ӧ��ѡ������������ʵ�ʹ�ҵ����ȴѡ��500�����ҵĸ��£�������ԭ�� ________��
(2)��֪��ҵ�̵���Ӧ��N2��g��+ 3H2��g��![]() 2NH3��g����H ����94.4kJ��mol��1������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼ1��ʾ����ʱ������վ���ƽ��״̬��
2NH3��g����H ����94.4kJ��mol��1������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼ1��ʾ����ʱ������վ���ƽ��״̬��
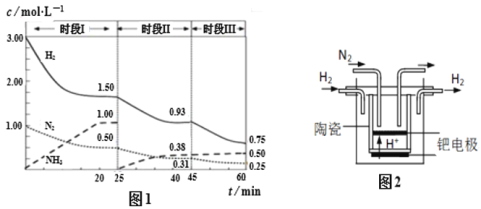
����2L�����з�����Ӧ��ǰ20min�ڣ���(NH3) �� ________��
��25 minʱ��ȡ��ij�ִ�ʩ�� ________��
��ʱ��III�����·�Ӧ��ƽ�ⳣ��Ϊ ________ L2�� mol��2(����3λ��Ч����) ��
(3)20����ĩ����ѧ�Ҳ��ø����ӵ����Ե�SCY�մ�(�ܴ���H+)Ϊ���ʣ�������������������ϵĽ����ٶྦྷ��Ĥ���缫��ʵ�ָ��³�ѹ�µĵ�ⷨ�ϳɰ�������˷�Ӧ���ת���ʣ���ʵ���ͼ��ͼ2��ʾ�������ĵ缫��Ӧʽ�� ________��
(4)���꣬���п�ѧ������ڳ��¡���ѹ�������������ºϳɰ�������˼·����Ӧԭ��Ϊ��2N2(g)+6H2O(l)![]() 4NH3(g)+3O2(g)�����䷴Ӧ����H �� ________����֪��N2(g)+ 3H2(g)
4NH3(g)+3O2(g)�����䷴Ӧ����H �� ________����֪��N2(g)+ 3H2(g)![]() 2NH3(g) ��H1 ����92.4kJ��mol��1 2H2(g) +O2(g)
2NH3(g) ��H1 ����92.4kJ��mol��1 2H2(g) +O2(g)![]() 2H2O(l) ��H2 ����571.6kJ��mol��1
2H2O(l) ��H2 ����571.6kJ��mol��1
����Ŀ��2SO2(g)+O2(g)![]() 2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ĸ����������Ϊ2 L�ĺ����ܱ�������Ͷ�ϣ�����ʼ���ʵ���������Ӧ���ƽ��ת�������±���ʾ��
2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ĸ����������Ϊ2 L�ĺ����ܱ�������Ͷ�ϣ�����ʼ���ʵ���������Ӧ���ƽ��ת�������±���ʾ��
�� | �� | �� | �� | ||
��ʼ���ʵ��� | n(SO2)/mol | 0.40 | 0 | 0.80 | 0.02 |
n(O2)/mol | 0.24 | 0 | 0.48 | 0.04 | |
n(SO3)/mol | 0 | 0.40 | 0 | 0.40 | |
����Ӧ���ƽ��ת����% | 80 |
|
|
| |
�����ж��У���ȷ����
A. ���¶��£�ƽ�ⳣ����ֵΪ400 B. ƽ��ʱ������c(SO3)�Ǽ��е�2��
C. ƽ��ʱ����3>��1 D. ����SO3��ƽ��ת����Ϊ��1 = 20%


