题目内容
14.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定为+m
A
解析:本题主要考查同主族元素的性质递变规律。由于X、Y原子的最外层电子数相同,且X的原子半径小于Y,所以X、Y同主族,且X位于Y的上面。由于同主族元素最高价氧化物对应水化物碱性从上到下逐渐增强,A正确;我们知道HNO3为强酸而氨水呈碱性,则B不正确;第ⅤA族元素氮的单质为N2,而硫的单质却有S8、S6、S4、S2等形式,C不正确;第ⅥA族元素,氧无正化合价,而硫的最高正价为+6,故D不正确。

(14分)阅读下表中的相关信息。除N外,其余都是主族元素。
| 元素代号 | 相关信息 |
| T | T的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X | X的原子2p轨道未成对电子数和成对电子数相等 |
| Y | 在第三周期元素中,Y的简单离子半径最小 |
| Z | T、X、Z组成的36电子的化合物A是家用消毒剂的主要成分 |
| M | M的氧化物是制造光导纤维的重要原料 |
| N | 位于第四周期,是人类最早使用的金属之一,单质呈红色 |
请按要求回答:
(1)元素T与X按原子个数比1∶1形成的化合物中所含的化学键类型有
,元素M与X形成的化合物B属于 晶体(填写晶体类型)。
(2)写出N基态原子电子排布式: 。
(3)元素T、Y、Z对应的单质的熔点高低顺序: > > (填化学式)。
(4)元素X、Y形成的简单离子半径大小: > (填相应的离子)。
(5)向Y与Z形成的化合物的水溶液中,加入过量T的最高价氧化物对应水化物的溶液,写出该反应的离子方程式: 。
(6) 一定条件下,X、Y两种单质以及有孔惰性电极在化合物TZ的水溶液中可形成原电池,为新型海水航标灯提供能源,该电池正极电极反应是: 。
 可与Y的应生成单质C,该反应的化学方程式为____________________。
可与Y的应生成单质C,该反应的化学方程式为____________________。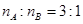 ),W的空间构型为_______________,工业上合成W气体选择的条件是________________。
),W的空间构型为_______________,工业上合成W气体选择的条件是________________。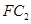 气体和3mol C的气体单质,一定条件下反应后生成
气体和3mol C的气体单质,一定条件下反应后生成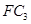 气体,当反应达到平衡时,单质C的浓度为
气体,当反应达到平衡时,单质C的浓度为 ,则平衡时
,则平衡时