题目内容
【题目】V L Fe2(SO4)3溶液中含有ag SO42-,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量浓度为( )
A.![]() mol·L-1B.
mol·L-1B.![]() mol·L-1C.
mol·L-1C.![]() mol·L-1D.
mol·L-1D.![]() mol·L-1
mol·L-1
【答案】A
【解析】
根据n=![]() 计算出ag硫酸根离子的物质的量,再根据硫酸铁的化学式计算出铁离子的物质的量,再计算出0.5vL溶液中含有的铁离子的物质的量;结合溶液稀释过程中铁离子的物质的量不变,根据c=
计算出ag硫酸根离子的物质的量,再根据硫酸铁的化学式计算出铁离子的物质的量,再计算出0.5vL溶液中含有的铁离子的物质的量;结合溶液稀释过程中铁离子的物质的量不变,根据c=![]() 计算出稀释后的铁离子的物质的量。
计算出稀释后的铁离子的物质的量。
ag SO42-的物质的量为:n(SO42-)=![]() mol,则VL该硫酸铁溶液中含有的Fe3+的物质的量为:n(Fe3+)=
mol,则VL该硫酸铁溶液中含有的Fe3+的物质的量为:n(Fe3+)=![]() n(SO42-)=
n(SO42-)=![]() ×
×![]() mol=
mol=![]() mol,0.5VL该溶液中含有铁离子的物质的量为:n(Fe3+)=
mol,0.5VL该溶液中含有铁离子的物质的量为:n(Fe3+)=![]() ×
×![]() mol=
mol=![]() mol,由于在稀释过程中铁离子的物质的量不变,则稀释后溶液中铁离子的浓度为:c(Fe3+)=
mol,由于在稀释过程中铁离子的物质的量不变,则稀释后溶液中铁离子的浓度为:c(Fe3+)=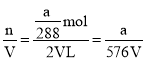 mol/L。
mol/L。
故合理选项是A。

练习册系列答案
相关题目














