题目内容
【题目】新型储氢材料是开发利用氢能源的关键因素。请回答下列问题:
(1)可以通过氢键形成“笼状结构”而成为潜在储氢材料的是_________(填标号)。
A.CH4 B.H2O C.HF D.H2S
(2)Ti(BH4)3是一种新型储氢材料。
①基态Ti3+的未成对电子数有______个。
②BH4-的空间构型是_________,其中B原子的杂化轨道类型为__________。
③写出一个与BH4-互为等电子体的物质的化学式_________。
④B、C、N、O的第一电离能由大到小顺序为_________。
(3)铁镁合金是目前已发现的储氢密度最高的材料之一
①亚铁离子基态核外电子排布式为__________。
②镁的电离能数据为:I1=738 kJ·mol-1,I2=1451 kJ·mol-1,I3=7733 kJ·kJ·mol-1,I4=10540 kJ·mol-1,I3>>I2的原因是________。
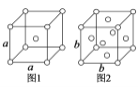
③铁单质有两种堆积方式,如图1和图2所示,边长分别为a、b,二者密度之比为________。
【答案】B 1 正四面体 sp3 CH4 N>O>C>B 1s22s22p63s23p63d6或[Ar]3d6 Mg失去2个电子后达到8电子稳定状态,故I3>>I2 b3:2a3
【解析】
(1)“可燃冰”甲烷水合物就是甲烷分子固定在水分子通过氢键形成的笼状结构中,由此推断出,该笼状结构也有可能储存氢气,故选B;
(2)①基态Ti原子的价电子排布为3d24s2,变为Ti3+后价电子为3d1,只有一个未成对电子,故答案为:1;②根据价层电子对互斥理论,BH4-中B有4个价电子,形成了4个σ键,没有孤电子对,所以空间构型为:正四面体形;B原子的杂化轨道类型为sp3,故答案为:正四面体;sp3;③与BH4-互为等电子体的物质应该是5个原子,共有8个价电子,符合的物质有:CH4,故答案为:CH4;
④N原子为半充满结构,第一电离能比O大,故B、C、N、O的第一电离能由大到小顺序为:N>O>C>B;
(3)①铁失去2个最外层电子变为亚铁离子,亚铁离子基态核外电子排布式为:1s22s22p63s23p63d6或[Ar]3d6;②Mg最外层有2个电子,Mg失去2个电子后达到8电子稳定状态,故I3>>I2;③由图1
可知a晶胞中包含了2个Fe原子,故a的密度为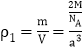 ;b晶胞中包含了4个Fe原子,故b的密度为
;b晶胞中包含了4个Fe原子,故b的密度为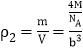 ;密度之比
;密度之比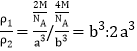 ;故答案为: 1s22s22p63s23p63d6或[Ar]3d6;Mg失去2个电子后达到8电子稳定状态,故I3>>I2;b3:2a3。
;故答案为: 1s22s22p63s23p63d6或[Ar]3d6;Mg失去2个电子后达到8电子稳定状态,故I3>>I2;b3:2a3。

【题目】下面a~e是中学化学实验中常见的几种定量仪器:a.量筒 b.容量瓶 c.滴定管 d.托盘天平 e.温度计
(1)无“0”刻度的是________(填字母)。
(2)下列操作合理的是________(填字母)。
A.用25 mL碱式滴定管量取20.00 mL NaHCO3溶液
B.用托盘天平准确称量10.20 g碳酸钠固体
C.用100 mL量筒量取3.2 mL浓硫酸
D.用500 mL容量瓶配制1 mol·L-1的氢氧化钠溶液495.5 mL
(3)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,若滴定开始和结束时,酸式滴定管中的液面如图所示:则所用盐酸的体积为________mL。
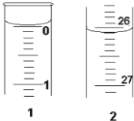
(4)某学生根据三次实验分别记录有关数据如下表:
滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理数据列出该氢氧化钠溶液物质的量浓度(计算结果保留4位有效数字):c(NaOH)=________ mol·L-1。
(5)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是________(填字母)。
A.中和滴定达终点时俯视滴定管内液面读数
B.碱式滴定管用蒸馏水洗净后立即取用25.00 mL待测碱溶液注入锥形瓶进行滴定
C.酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定
D.把配好的标准溶液倒入刚用蒸馏水洗净的试剂瓶中然后用来滴定