题目内容
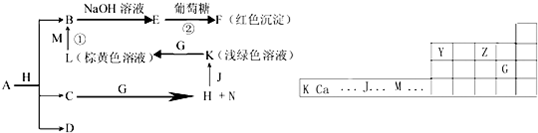
已知常温下X为无色液体,D、E均为无色气体,G是一种重要的工业产品.C的焰色反应为黄色,E、F的相对分子质量之间的关系为M(F)=M(E)+16.试回答下列问题:
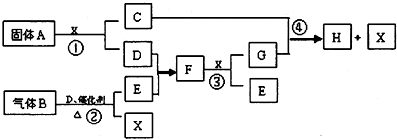
(1)A中所含化学键的类型为 ,写出B的一个用途 .
(2)将固体A加入CuSO4溶液中的主要现象是 .
(3)写出气体B的水溶液与CuSO4溶液反应的离子方程式: .
(4)写出反应②的化学方程式,若是氧化还原反应,请标出电子转移的方向和数目: .
(5)经测定,反应④中每生成1.0g X,放出3.2kJ的热量(常温下).试写出反应④的热化学方程式: .

(1)A中所含化学键的类型为
(2)将固体A加入CuSO4溶液中的主要现象是
(3)写出气体B的水溶液与CuSO4溶液反应的离子方程式:
(4)写出反应②的化学方程式,若是氧化还原反应,请标出电子转移的方向和数目:
(5)经测定,反应④中每生成1.0g X,放出3.2kJ的热量(常温下).试写出反应④的热化学方程式:
分析:已知常温下X为无色液体,D、E均为无色气体,C的焰色反应为黄色说明含有钠元素,固体A和X反应生成的气体D为氧气,确定A为Na2O2,X为H2O,D为O2,C为NaOH;G是一种重要的工业产品,和氢氧化钠反应生成水和H,说明G为酸,E、F的相对分子质量之间的关系为M(F)=M(E)+16,说明EF为非金属氧化物,结合反应F+X=G+E,分析判断,G为HNO3,E为NO,F为NO2,气体B催化氧化加热生成一氧化氮和水的反应是氨气的催化氧化反应,推断B为NH3;依据推断结果回答问题;
解答:解:C的焰色反应为黄色说明含有钠元素,固体A和X反应生成的气体D为氧气,已知常温下X为无色液体,确定A为Na2O2,X为H2O,D为O2,C为NaOH;G是一种重要的工业产品,和氢氧化钠反应生成水和H,说明G为酸,E、F的相对分子质量之间的关系为M(F)=M(E)+16,说明EF为非金属氧化物,结合反应F+X=G+E,D、E均为无色气体,分析判断,G为HNO3,E为NO,F为NO2,气体B催化氧化加热生成一氧化氮和水的反应是氨气的催化氧化反应,推断B为NH3;
(1)A为Na2O2所含化学键的类型为离子键、非极性共价键;B为NH3,主要作用有制备硝酸,做制冷剂等;
故答案为:离子键、非极性共价键;制备硝酸,做制冷剂,制备氮肥等
(2)将固体A为Na2O2加入CuSO4溶液中,钠和水反应生成氢氧化钠和氢气,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,反应的主要现象是有无色气体生成,有蓝色沉淀氢氧化铜生成;
故答案为:无色气体,蓝色沉淀;
(3)气体B为氨气,氨气的水溶液为一水合氨,与CuSO4溶液反应的离子方程式为:2NH3?H2O+Cu2+=Cu(OH)2↓+2NH4+;
故答案为:2NH3?H2O+Cu2+=Cu(OH)2↓+2NH4+;
(4)反应②是氨气的催化氧化反应,配平写出反应的化学方程式,以及以上化合价变化标注氧化还原反应地址转移数目,得到化学方程式为: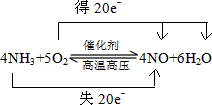 ;
;
故答案为: ;
;
(5)反应④为NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l),反应中每生成1.0g X为H2O,放出3.2kJ的热量(常温下),生成18g水放热为18g×3.2kJ=57.6KJ;反应的热化学方程式为:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l);△H=-57.6kJ/mol;
故答案为:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l);△H=-57.6kJ/mol;
(1)A为Na2O2所含化学键的类型为离子键、非极性共价键;B为NH3,主要作用有制备硝酸,做制冷剂等;
故答案为:离子键、非极性共价键;制备硝酸,做制冷剂,制备氮肥等
(2)将固体A为Na2O2加入CuSO4溶液中,钠和水反应生成氢氧化钠和氢气,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,反应的主要现象是有无色气体生成,有蓝色沉淀氢氧化铜生成;
故答案为:无色气体,蓝色沉淀;
(3)气体B为氨气,氨气的水溶液为一水合氨,与CuSO4溶液反应的离子方程式为:2NH3?H2O+Cu2+=Cu(OH)2↓+2NH4+;
故答案为:2NH3?H2O+Cu2+=Cu(OH)2↓+2NH4+;
(4)反应②是氨气的催化氧化反应,配平写出反应的化学方程式,以及以上化合价变化标注氧化还原反应地址转移数目,得到化学方程式为:
 ;
;故答案为:
 ;
;(5)反应④为NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l),反应中每生成1.0g X为H2O,放出3.2kJ的热量(常温下),生成18g水放热为18g×3.2kJ=57.6KJ;反应的热化学方程式为:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l);△H=-57.6kJ/mol;
故答案为:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l);△H=-57.6kJ/mol;
点评:本题考查了物质转化关系的分析应用,物质性质和特征反应以及反应现象的分析是解题关键,注意氮及其化合物转化关系的特征应用,物质性质的熟练掌握,题目难度中等.

练习册系列答案
相关题目