题目内容
周期表中有六种元素,其中X的原子半径最小,Y、Z、G、J、M五种元素的位置如下所示,C、D是由X、Y、Z中两种元素组成的化合物,C通常状况下为无色液体,D为无色非可燃性气体,常温下G为有颜色的单质气体,各物质之间的转换关系如下图,部分生成物省略.N有漂白作用,反应①常用于制作印刷电路板.
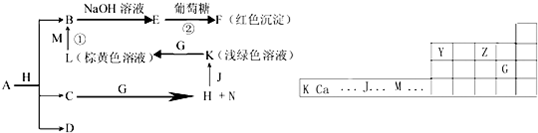
请回答下列问题:
(1)写出由四种元素组成的化合物A的化学式 ,C分子的电子式 .
(2)反应②在医学上有重要的应用,可用于检验病人尿液的葡萄糖是否存在,请写出反应②的化学方程式 .
(3)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体.请写出该反应的化学方程式: .

请回答下列问题:
(1)写出由四种元素组成的化合物A的化学式
(2)反应②在医学上有重要的应用,可用于检验病人尿液的葡萄糖是否存在,请写出反应②的化学方程式
(3)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体.请写出该反应的化学方程式:
分析:周期表中有六种元素,其中X的原子半径最小,则X为H元素;由Y、Z、G、J、M五种元素的位置可知,Y为C,Z为O、G为Cl,J、M都是过渡元素金属,
G的单质是黄绿色单质,所以G单质为Cl2;C、D是由H、C、O中两种元素组成的化合物,C通常状况下为无色液体,与Cl2生成H和I,I有漂白作用,所以C为H2O,H为HCl,I为HClO;HCl与金属J反应得到K,为淡绿色溶液,所以J为Fe,K为FeCl2,FeCl2与Cl2反应生成L,L为FeCl3;反应①用于制作印刷电路板,为FeCl3和Cu反应,则M为Cu,B为CuCl2,E能与葡萄糖反应,应为Cu(OH)2,故F为Cu2O.反应A+H(HCl)=B(CuCl2)+C(H2O)+D中,D是无色非可燃性气体,应为CO2,可推知A是含有Cu2+的碳酸盐,应为CuCO3或Cu2(OH)2CO3,题中告诉“A是含有四种元素的化合物”,可知A应为Cu2(OH)2CO3,结合相关物质的性质解答该题.
G的单质是黄绿色单质,所以G单质为Cl2;C、D是由H、C、O中两种元素组成的化合物,C通常状况下为无色液体,与Cl2生成H和I,I有漂白作用,所以C为H2O,H为HCl,I为HClO;HCl与金属J反应得到K,为淡绿色溶液,所以J为Fe,K为FeCl2,FeCl2与Cl2反应生成L,L为FeCl3;反应①用于制作印刷电路板,为FeCl3和Cu反应,则M为Cu,B为CuCl2,E能与葡萄糖反应,应为Cu(OH)2,故F为Cu2O.反应A+H(HCl)=B(CuCl2)+C(H2O)+D中,D是无色非可燃性气体,应为CO2,可推知A是含有Cu2+的碳酸盐,应为CuCO3或Cu2(OH)2CO3,题中告诉“A是含有四种元素的化合物”,可知A应为Cu2(OH)2CO3,结合相关物质的性质解答该题.
解答:解:期表中有六种元素,其中X的原子半径最小,则X为H元素;由Y、Z、G、J、M五种元素的位置可知,Y为C,Z为O、G为Cl,J、M都是过渡元素金属,
G的单质是黄绿色单质,所以G单质为Cl2;C、D是由H、C、O中两种元素组成的化合物,C通常状况下为无色液体,与Cl2生成H和I,I有漂白作用,所以C为H2O,H为HCl,I为HClO;HCl与金属J反应得到K,为淡绿色溶液,所以J为Fe,K为FeCl2,FeCl2与Cl2反应生成L,L为FeCl3;反应①用于制作印刷电路板,为FeCl3和Cu反应,则M为Cu,B为CuCl2,E能与葡萄糖反应,应为Cu(OH)2,故F为Cu2O.反应A+H(HCl)=B(CuCl2)+C(H2O)+D中,D是无色非可燃性气体,应为CO2,可推知A是含有Cu2+的碳酸盐,应为CuCO3或Cu2(OH)2CO3,题中告诉“A是含有四种元素的化合物”,可知A应为Cu2(OH)2CO3,
(1)由上述分析可知,A为Cu2(OH)2CO3,C为H2O,分子中O原子与H原子之间形成1对共用电子对,其电子式为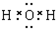 ,
,
故答案为:Cu2(OH)2CO3;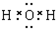 ;
;
(2)反应②的化学方程式为:CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+Cu2O↓+2H2O,
故答案为:CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+Cu2O↓+2H2O;
(3)F为Cu2O,与稀硝酸反应生成硝酸铜和NO,反应方程式为3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O,
故答案为:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O.
G的单质是黄绿色单质,所以G单质为Cl2;C、D是由H、C、O中两种元素组成的化合物,C通常状况下为无色液体,与Cl2生成H和I,I有漂白作用,所以C为H2O,H为HCl,I为HClO;HCl与金属J反应得到K,为淡绿色溶液,所以J为Fe,K为FeCl2,FeCl2与Cl2反应生成L,L为FeCl3;反应①用于制作印刷电路板,为FeCl3和Cu反应,则M为Cu,B为CuCl2,E能与葡萄糖反应,应为Cu(OH)2,故F为Cu2O.反应A+H(HCl)=B(CuCl2)+C(H2O)+D中,D是无色非可燃性气体,应为CO2,可推知A是含有Cu2+的碳酸盐,应为CuCO3或Cu2(OH)2CO3,题中告诉“A是含有四种元素的化合物”,可知A应为Cu2(OH)2CO3,
(1)由上述分析可知,A为Cu2(OH)2CO3,C为H2O,分子中O原子与H原子之间形成1对共用电子对,其电子式为
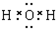 ,
,故答案为:Cu2(OH)2CO3;
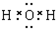 ;
;(2)反应②的化学方程式为:CH2OH(CHOH)4CHO+2Cu(OH)2
| △ |
故答案为:CH2OH(CHOH)4CHO+2Cu(OH)2
| △ |
(3)F为Cu2O,与稀硝酸反应生成硝酸铜和NO,反应方程式为3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O,
故答案为:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O.
点评:本题考查无机物的推断,主要涉及Cu、Fe、Cl元素单质及化合物性质,综合性较大,要掌握常见元素及其单质和化合物的性质,题目中包含有机物知识的渗透,侧重对知识迁移以及学生综合能力的考查过程,难度较大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(15分)六种短周期元素在周期表中的相对位置如下所示,其中E元素原子核外电子总数是其最外层电子数的3倍。关于元素周期表及这六种元素性质,请回答:
| A | B | C |
| D | E | F |
(2) AC2的结构式为________;
(3) 在一定条件下,由B单质与H2反应生成1 molG时,放出的热量为46.2 kJ,写出该反应的热化学方程式:______________________________
(4) 工业上用G检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,写出化学方程式____________________________________
该反应中被氧化的G与参与反应的G的质量之比________。



 【化学一一选修物质结构与性质】
【化学一一选修物质结构与性质】