题目内容
【题目】人体内最重要的供能物质是
A.葡萄糖 B.纤维素 C.油脂 D.蛋白质
【答案】A
【解析】
试题糖类是人体的能量的重要来源,葡萄糖属于糖类,所以选A。

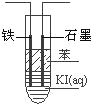
【题目】I. 为比较Cl2、Fe3+、SO2的氧化性,用下图所示装置进行实验,其过程如下:

①.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
②.打开活塞a,滴加一定量的浓盐酸,给A加热。
③.当B中的溶液变黄时,停止加热,夹紧弹簧夹K2。
④.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
⑤.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
⑥.更新试管D,重复过程④,检验B溶液中的离子。
(1)棉花中浸润的溶液为__________。
(2)当A中足量固体加入36.5%密度为1.2g/mL盐酸100mL时,其反应转移的电子数目为______。
(3)过程⑥中检验B溶液中是否含有硫酸根离子的操作是___________。
(4)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性的是____同学,其氧化性顺序为____________。
过程④ B溶液中含有的离子 | 过程⑥ B溶液 中含有的离子 | |
甲 | 有Fe3+无Fe2+ | 有SO42- |
乙 | 既有Fe3+又有Fe2+ | 有SO42- |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |
II. NaNO2是重要的防腐剂,+3价的氮易发生氧化反应且在酸性环境中不稳定。其5mol/L水溶液pH为9。某化学兴趣小组设计如下图所示装置制备亚硝酸钠。其操作是①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;②一段时间后停止加热。回答下列问题:

(1)B中观察的主要现象是__________,D装置的作用是____________。
(2)检验C中产物有亚硝酸钠的操作是_______,相应反应方程式为___________。
(3)经检验C中产物亚硝酸钠含量较少。a. 甲同学认为C中产物不仅有亚硝酸钠,还有其他杂质。为排除干扰,甲在B、C装置间增加装置E,E中盛放的试剂是_______(写名称)。b. 乙同学认为除上述干扰因素外,还会有氧气参与反应导致产品不纯,所以在实验操作①前应增加一步操作,该操作是___。
(4)由题给条件计算HNO2的Ka数值为______________。