��Ŀ����
����Ŀ����������(ClO2)��һ����ˮ�����ȷ����й㷺Ӧ�õĸ�Ч��ȫ��������������Cl2��Ȳ��������������DZ��Σ�����л��ȴ����֪: ClO2Ũ�ȹ��������ֽ⣬�����ᱬը�����������Ʊ�ClO2�ķ���:
��1������һ��������
�����������ƺ�ϡ����Ϊԭ���Ʊ�����Ӧԭ��Ϊ5NaClO2+4HCl=5NaCl+4ClO2��+2H2O��
�ٸ÷�Ӧ���������ͻ�ԭ�������ʵ���֮����_______________________��
���о�����������Ӧ��ʼʱ����Ũ�Ƚϴ��������������Cl2�������ӷ���ʽ���Ͳ���Cl2��ԭ��__________��
��2�����������Ȼ��Ƶ�ⷨ
�����ڵ���ʳ��ˮ���ȳ�ȥ���е�Ca2+��Mg2+��SO42-�����ʡ�ij�γ��Ӳ���ʱ��������ˮ���ȼ��������____���ѧʽ�������������ٲ������ټ��������Na2CO3��NaOH����ַ�Ӧ����һ����ȥ��
�ڸ÷�����ԭ��ʾ��ͼ��ͼ��ʾ��������ǽ�ʳ��ˮ���ض������µ��õ��������ƣ�NaClO3�������ᷴӦ����ClO2���Ȼ��Ƶ����з�����Ӧ�Ļ�ѧ����ʽΪ_____________��

��3�������������ỹԭ��
��������Һ���ò��ᣨH2C2O4����ԭ�����Ƶķ������Ʊ�ClO2
��д���Ʊ�ClO2�����ӷ���ʽ��____________________��
�����ⷨ��ȣ��ò��ỹԭ���Ʊ�ClO2���ص���____________________����������������漰������̵İ�ȫ�ԡ�
��4����֪: ClO2��I-��ԭΪClO2-��Cl-��ת��������ҺpH �Ĺ�ϵ��ͼ��ʾ����pH<2.0 ʱ��ClO2-Ҳ�ܱ�I- ��ȫ��ԭΪCl-����Ӧ���ɵ�I2��Na2S2O3 ��Ӧ�ķ���ʽ: 2Na2S2O3+ I2= Na2S4O6 + 2NaI��
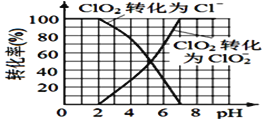
��ClO2����������ˮ�к���ClO2��ClO2-���ⶨ����ˮ��ClO2��ClO2-�ĺ���������������:
��������ֹ��ȷ����ˮ����ClO2�ĺ���Ϊa mol/L��
���õζ�������ClO2-�ĺ������������Ӧ��ʵ�鲽��:
����1: ȷ��ȡV mL ����ˮ��������ƿ�С�
����2: ����ˮ����pH________��
����3: ����������KI ���壬��ַ�Ӧ��
����4: ��������������Һ����c mol/L Na2S2O3 ��Һ�ζ����յ㣬����Na2S2O3 ��ҺV1 mL��
���������������ݣ���ø�����ˮ��ClO2-��Ũ��Ϊ________mol/L( �ú���ĸ�Ĵ���ʽ��ʾ)��
���𰸡�1��4 4H++ClO2-+3Cl-=2Cl2��+2H2O BaCl2 NaCl+3H2O ![]() NaClO3+ H2�� 2ClO3 - + H2C2O4+ 2H+ =2ClO2�� + 2CO2�� + 2H2O ���ɵ�CO2��ClO2��ϡ������ ��2.0 (cV1-5aV) /4V
NaClO3+ H2�� 2ClO3 - + H2C2O4+ 2H+ =2ClO2�� + 2CO2�� + 2H2O ���ɵ�CO2��ClO2��ϡ������ ��2.0 (cV1-5aV) /4V
��������
(1)��NaClO2�����绯��Ӧ���������������ǻ�ԭ����HCl��������ã�����������NaClO2ת��ΪNaCl������������NaClO2ת��ΪClO2��5molNaClO2��Ӧ����4mol ClO2��5mol NaCl������4molNaCl��HClת���õ�����NaClO2ת���õ�1molNaCl���ʷ�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ1��4���ʴ�Ϊ��1��4��
��ClO2-����ǿ�����ԣ�������������Cl-��Ӧ����������ͬʱ������ˮ����Ӧ���ӷ���ʽΪ��4H++ClO2-+3Cl-=2Cl2��+2H2O���ʴ�Ϊ��4H++ClO2-+3Cl-=2Cl2��+2H2O��
(2)���ڳ��ӵĹ�����ÿ��������Լ������ǹ����ģ�ʹ���ӳ����������������ں��������б����ȥ��������BaCl2���ڳ�ȥSO42-��������NaOH��Һ����ȥMg2+��������Na2CO3��ȥCa2+��������Ba2+�����˺���Һ�������ȥ������Na2CO3��NaOH���ʳ�������ʱ��̼���Ƽ���Ӧ���Ȼ���֮��NaOH����˳��û��Ҫ�ʣ�������ˮ���ȼ��������BaCl2�����������ٲ������ټ��������Na2CO3��NaOH����ַ�Ӧ����һ����ȥ���ʴ�Ϊ��BaCl2��
�ڵ��ʳ��ˮ�õ���������(NaClO3)���ɵ���ת���غ��֪��������������ɣ�NaClO3�����ᷴӦ����ClO2���е�����������Ȼ��Ƶ���ѭ�����ã�˵����NaCl���ɣ��е����������HCl�ϳ�����ѭ�����ã�˵���������������������ȷ�����������ClO2�Ļ�ѧ����ʽΪ��2NaClO3+4HCl=2ClO2��+Cl2��+2NaCl+2H2O������Ȼ��Ƶ����з�����ӦΪ����Ȼ������������ƺ���������ѧ����ʽΪ��NaCl+3H2O ![]() NaClO3+3H2�����ʴ�Ϊ��NaCl+3H2O
NaClO3+3H2�����ʴ�Ϊ��NaCl+3H2O ![]() NaClO3+3H2����
NaClO3+3H2����
(3)���������ữ�IJ���(H2C2O4)��Һ��ԭ�����ƣ���Ӧ���������ơ�������̼���������ȡ�ˮ���÷�ӦΪH2C2O4+2NaClO3+H2SO4�TNa2SO4+2CO2��+2ClO2��+2H2O�����ӷ�ӦΪH2C2O4+2ClO3-+2H+=2CO2��+2ClO2��+2H2O���ʴ�Ϊ��H2C2O4+2ClO3-+2H+=2CO2��+2ClO2��+2H2O��
�ڸ������⣬ClO2Ũ�ȹ��������ֽ⣬�����ᱬը���˷���Ӧ���������ɵĶ�����̼��ϡ�����ã���������������桢����İ�ȫ�ԣ��ʴ�Ϊ�����ɵ�CO2��ClO2��ϡ�����ã�
(4)����4��Na2S2O3�ζ���Һ��I2������2��Ҫ����pHʹClO2-��I-����ΪI2����Ӧ����pH��2.0��V mL��Һ�У�ClO2�����ʵ���Ϊ=V��10-3 L��a mol/L=aV��10-3 mol���ɵ���ת���غ�ɵã�2 ClO2��5 I2��ClO2��������I2�����ʵ���=2.5aV��10-3 mol������Na2S2O3�����ʵ���=V1��10-3 L��cmol/L=cV1��10-3 mol����2Na2S2O3+I2=Na2S4O6+2NaI����Һ��I2�����ʵ���=0.5 cV1��10-3 mol��ClO2-�������ɵ�I2�����ʵ���=0.5 cV1��10-3 mol-2.5aV��10-3 mol=(0.5 cV1-2.5aV)��10-3 mol���ɵ���ת���غ�ɵã�ClO2-��2I2����ClO2-�����ʵ���= ![]() ��(0.5 cV1-2.5aV)��10-3 mol����c(ClO2-)=
��(0.5 cV1-2.5aV)��10-3 mol����c(ClO2-)= ![]() ��(0.5 cV1-2.5aV)��10-3 mol��V��10-3 L=
��(0.5 cV1-2.5aV)��10-3 mol��V��10-3 L= ![]() mol/L���ʴ�Ϊ����2.0��
mol/L���ʴ�Ϊ����2.0��![]() ��
��