题目内容
【题目】为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
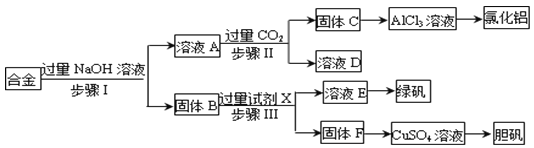
请回答:
(1)写出步骤Ⅰ反应的离子方程式:_________________________。
(2)试剂X是______。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是________。
(3)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式_______________________________,请选出你认为的最佳途径并说明选择的理由______________________________。
【答案】 2Al+2OH—+2H2O=2AlO2-+3H2↑ 稀硫酸或H2SO4 过滤 3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O 途径②最佳,理由是原料利用率高,环境污染小
【解析】铝、铁和铜的合金中只有金属铝可以和氢氧化钠反应,过滤后,得到溶液A含有NaOH、NaAlO2,固体B为Cu和Fe。溶液A中通入过量的二氧化碳可以得到氢氧化铝沉淀与碳酸氢钠,过滤分离,得到C为Al(OH)3,D为NaHCO3溶液,氢氧化铝溶解在盐酸中得到氯化铝溶液,然后蒸发结晶得到氯化铝固体。固体B用试剂X反应,过滤分离得到溶液E,溶液E蒸发浓缩、冷却结晶可以获得绿矾晶体,可知试剂X为稀硫酸,E为FeSO4,F为Cu,Cu转化得到硫酸铜,CuSO4溶液蒸发浓缩、冷却结晶可以获得胆矾晶体,据此解答。
(1)步骤Ⅰ中铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应的离子方程式为2Al+2OH—+2H2O=2AlO2-+3H2↑;
(2)由上述分析可知,试剂X为稀硫酸,步骤Ⅰ、Ⅱ、Ⅲ均是固体和液体的分离操作,应该是过滤;
(3)途径①中Cu与混酸反应生成铜盐、NO与水,反应的离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;途径①产生NO,途径③中会生成二氧化硫,NO、二氧化硫均污染空气,铜不能和稀硫酸反应,但是当加热并通入空气之后,铜和氧气反应生成氧化铜,然后氧化铜会和硫酸反应生成硫酸铜,不会产生污染大气的气体,该过程原料利用率高,所以途径②最佳。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案【题目】(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2(g)+3H2(g)![]() 2NH3(g)。该可逆反应达到平衡的标志是________。
2NH3(g)。该可逆反应达到平衡的标志是________。
A.3v正(H2)=2v逆(NH3) B.单位时间生成m mol N2的同时生成3m mol H2
C.容器内的总压强不再随时间而变化 D.混合气体的密度不再随时间变化
(2)工业上可用天然气为原料来制取合成氨的原料气氢气。某研究性学习小组的同学模拟工业制取氢气的原理,在一定温度下,体积为2 L的恒容密闭容器中测得如下表所示数据。请回答下列问题:
时间/min | CH4/mol | H2O/mol | CO/mol | H2/mol |
0 | 0.40 | 1.00 | 0 | 0 |
5 | a | 0.80 | c | 0.60 |
7 | 0.20 | b | 0.20 | d |
分析表中数据,判断5 min时反应是否处于平衡状态?______(填“是”或“否”),前5 min反应的平均反应速率v(CH4)=____________________。
(3)恒温恒容下,将2 mol 气体A和2 mol气体B通入体积为2L的密闭容器中,发生如下反应:2A(g)+B(g) xC(g)+2D(s),2 min后反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol/L。
①x=________。
②A的转化率与B的转化率之比为________。