题目内容
硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离.但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:H2SO4═H++HSO4-,HSO4-?H++SO42-.
请回答下列有关问题:
(1)K2SO4溶液呈 (填“弱酸性”、“中性”或“弱碱性”),其理由是 (用离子方程式表示).
(2)NaHSO4溶液与NaHCO3溶液反应的离子方程式为 .
(3)若25℃时,0.10mol?L-1的NaHSO4溶液中c(SO42-)=0.029mol?L-1,则HSO4-的电离常数Ka= (保留两位有效数字);0.10mol?L-1的H2SO4溶液中c(H+) 0.129mol?L-1(填“>”、“=”或“<”).
请回答下列有关问题:
(1)K2SO4溶液呈
(2)NaHSO4溶液与NaHCO3溶液反应的离子方程式为
(3)若25℃时,0.10mol?L-1的NaHSO4溶液中c(SO42-)=0.029mol?L-1,则HSO4-的电离常数Ka=
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:(1)硫酸钾中硫酸根离子能水解、钾离子不水解;
(2)二者反应生成硫酸钠、二氧化碳和水;
(3)根据电离平衡常数公式计算;硫酸电离出的氢离子抑制硫酸氢根离子电离.
(2)二者反应生成硫酸钠、二氧化碳和水;
(3)根据电离平衡常数公式计算;硫酸电离出的氢离子抑制硫酸氢根离子电离.
解答:
解:(1)硫酸钾中硫酸根离子能水解、钾离子不水解,所以硫酸钾溶液呈弱碱性,水解离子方程式为SO42-+H2O?HSO4-+OH-,故答案为:弱碱性;SO42-+H2O?HSO4-+OH-;
(2)二者反应生成硫酸钠、二氧化碳和水,离子方程式为HSO4-+HCO3-=H2O+CO2↑+SO42-,故答案为:HSO4-+HCO3-=H2O+CO2↑+SO42-;
(3)0.10mol?L-1的NaHSO4溶液中c(SO42-)=0.029mol?L-1,溶液中c(H+)=c(SO42-)=0.029mol?L-1,则HSO4-的电离常数Ka=
=0.012,硫酸第一步电离的氢离子抑制硫酸氢根离子电离,所以溶液中c(H+)<0.129mol?L-1,故答案为:0.012;<.
(2)二者反应生成硫酸钠、二氧化碳和水,离子方程式为HSO4-+HCO3-=H2O+CO2↑+SO42-,故答案为:HSO4-+HCO3-=H2O+CO2↑+SO42-;
(3)0.10mol?L-1的NaHSO4溶液中c(SO42-)=0.029mol?L-1,溶液中c(H+)=c(SO42-)=0.029mol?L-1,则HSO4-的电离常数Ka=
| 0.029×0.029 |
| 0.10-0.029 |
点评:本题以信息给予为载体考查了弱电解质的电离,注意硫酸第二步电离特点,再结合电离平衡常数公式计算硫酸氢根离子电离平衡常数,为易错题.

练习册系列答案
相关题目
下列原理或操作不正确的是( )
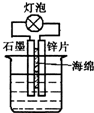

| A、在如图装置的稀硫酸中加入适量重铬酸钾或适量6%的H2O2溶液,可以使灯泡亮度增大,持续时间变长 |
| B、纸层析法分离微量成份时均需有以下流程:装置制作→点层析试样→配制展开剂→层析操作→显色反应 |
| C、在提纯混有少量NaCl的KNO3时,常先将混合物在较高温度下溶于水形成浓溶液,再经过冷却结晶、过滤、洗涤、干燥,获得KNO3晶体 |
| D、制摩尔盐时用酒精洗涤产品,用干净的滤纸吸干;而在制阿司匹林粗品时用冷水洗涤产品,在空气中风干 |
下列关于溶液的说法正确的是( )
| A、1L 0.2mol/L CaCl2溶液中,Cl-数目约为0.2×6.02×1023个 |
| B、50mL 1mol/L AlCl3溶液与100mL 3mol/L KClO3溶液中的Cl-物质的量浓度相等 |
| C、0.5L 1mol/L MgCl2溶液与0.2L 1mol/L KCl溶液中的Cl-的数目之比为5:2 |
| D、在100mL Na2SO4和KNO3的混合溶液中,Na+的物质的量浓度与SO42-的物质的量浓度之比为2:1 |