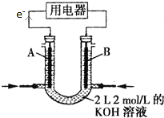
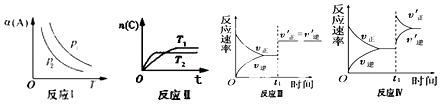
题目内容
【题目】某兴趣小组欲测定市场上某H2O2消毒液质量分数,现进行如下操作
己知:2MnO4﹣+5H2O2+6H+═2Mn2++8H2O+5O2
操作①:取10.00mLH2O2溶液(密度为1.00gmL﹣1)置于锥形瓶中加水稀释,再加稀硫酸酸化;
操作②:用0.200 0molL﹣1KMnO4溶液滴定;
操作③:用同样方法滴定,4次消耗KMnO4溶液的体积分别为20.00mL、19.98mL、20.02mL、22.00mL.请回答下列问题:
(1)滴定时盛装KMnO4溶液应选取的仪器是(填序号).
A.50mL酸式滴定管
B.50mL碱式滴定管
C.25mL酸式滴定管
D.25mL碱式滴定管
(2)是否需要选用指示剂(填“是”或“否”)达到滴定终点的现象是 .
(3)分析数据,计算该H2O2溶液中溶质的质量分数为(保留三位有效数字).
【答案】
(1)C
(2)否,滴入最后一滴酸性KMnO4溶液,溶液由无色变为紫红色,30秒内不恢复
(3)3.40%
【解析】解:(1)KMnO4溶液具有强氧化性,可以腐蚀橡皮管,故KMnO4溶液应装在酸式滴定管中,四次消耗KMnO4溶液的体积分别为20.00mL、19.98mL、20.02mL、22.00mL,所以选用25ml酸式滴定管可以完成实验,
所以答案是:C;
(2)KMnO4溶液为紫红色溶液,可以根据高锰酸钾溶液溶液颜色变化判断滴定终点,所以不需要指示剂;该滴定终点的现象为:滴入最后一滴酸性KMnO4溶液,溶液由无色变为紫红色,30秒内不恢复,说明反应结束,
所以答案是:否; 滴入最后一滴酸性KMnO4溶液,溶液由无色变为紫红色,30秒内不恢复;
(3)过氧化氢溶液中过氧化氢质量=5.0ml×1.0g/ml=5g,用0.1000mol/L KMnO4溶液滴定,用同样方法滴定,四次消耗KMnO4溶液的体积分别为20.00mL、19.98mL、20.02mL、22.00ml,第四次误差较大舍去,平均 消耗高锰酸钾溶液体积= ![]() =20.00mL,
=20.00mL,
根据反应 | 2MnO4﹣+ | 5H2O2+6H+=2Mn2++8H2O+5O2↑ |
2 | 5 | |
0.2000mol/L×0.02L | n(H2O2) |
![]() =
= ![]() ,解得:n(H2O2)=0.01mol,
,解得:n(H2O2)=0.01mol,
则过氧化氢质量分数为: ![]() ×100%=3.40%,
×100%=3.40%,
所以答案是:3.40%.
【考点精析】解答此题的关键在于理解酸碱中和滴定的相关知识,掌握中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准液;先用待测液润洗后在移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点.

【题目】I.现有三个反应:
反应①![]()
![]() =a kJ/mol平衡常数为K1
=a kJ/mol平衡常数为K1
反应②![]()
![]() 平衡常数为K2
平衡常数为K2
反应③![]()
![]() =b kJ/mol平衡常数为K3
=b kJ/mol平衡常数为K3
在不同温度下,部分K1、K2的值如下:
T/℃ | 700 | 800 |
K1 | 2.38 | 2.56 |
K2 | 0.80 |
(1) ![]()
![]() ==____________________
==____________________
(2)K1的表达式为____________;根据反应①、②、③推导出K1、K2、K3的关系式K3=______________。
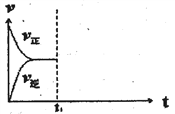
(3)在恒温恒压密闭容器中通入CO和H2O各1mol发生反应②,当反应达到平衡后,维持温度与压强不变,t1时再通入各1mol的CO和H2O的混合气体,请在下图中画出正(v正)、逆(v逆)反应速率在t1后随时间t变化的曲线图_______。
Ⅱ.在容积相同的两个密闭容器内(装有等量的某种催化剂),分别充入同量的NOx及C3H6,在不同温度下,同时发生以下反应:
18NO(g)+2C3H6(g) 9N2(g)+6CO2(g)+6H2O(g):
18NO2(g)+4C3H6(g) 9N2(g)+12CO2(g)+12H2O(g);
并分别在t秒时测定其中NOx转化率,绘得图像如下图所示:
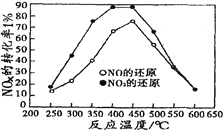
①从图中可以得出的结论是
结论一:从测定NOx转化数据中判断,相同温度下NO转化效率比NO2的低。
结论二:________________________________________________________
②在上述NO2和C3H6反应中,提高NO2转化率的措施有_____________。(填编号)
A.加入催化剂 B.降低温度 C.分离出H
Ⅲ.常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.6,c(H2CO3)=1.5×10 -5 mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3HCO3-+ H+ 的平衡常数K1=___________。(已知:10-5.60=2.5×10-6 )