题目内容
下列物质中,不属于电解质的是( )
| A、H2SO4 |
| B、Na2SO4 |
| C、乙醇 |
| D、Ba(OH)2 |
考点:电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物既不是电解质也不是非电解质.
解答:
解:A、H2SO4 为共价化合物,在水溶液中能电离出H+和SO42-而导电,属于电解质,故A不选;
B、Na2SO4为离子化合物,在水溶液中能电离出Na+和SO42-而导电,属于电解质,故B不选;
C、乙醇是共价化合物不导电,属非电解质,故C选;
D、Ba(OH)2为离子化合物,在水溶液中能电离出Ba2+和OH-而导电,属于电解质,故D不选;
故选C.
B、Na2SO4为离子化合物,在水溶液中能电离出Na+和SO42-而导电,属于电解质,故B不选;
C、乙醇是共价化合物不导电,属非电解质,故C选;
D、Ba(OH)2为离子化合物,在水溶液中能电离出Ba2+和OH-而导电,属于电解质,故D不选;
故选C.
点评:本题较简单,主要考查电解质的定义,熟悉常见的酸、碱、盐都属于电解质来解答.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列事实不能用勒沙特列原理解释的是( )
| A、氨水应密闭保存,放置低温处 |
| B、在FeCl2溶液中加入铁粉防止氧化变质 |
| C、常温下,将1mL pH=3的醋酸溶液加水稀释至100mL,测得其pH<5 |
| D、.实验室可用排饱和食盐水的方法收集氯气 |
下列说法中正确的是( )
| A、实验室用乙醇和浓硫酸按体积比3:1混合加热到170℃制乙烯 |
| B、苯酚有杀菌和止痛作用,有些药皂中也掺入了少量的苯酚,所以我们可以将苯酚用于环境消毒或直接涂抹于皮肤上起消毒作用 |
| C、工业酒精不能加水而当美酒品尝,因其中含有甲醇,它虽也具有酒香气味,但饮后会造成人的双目终身失明或致死 |
| D、通常用来衡量一个国家的石油化学工业发展水平的标志是汽油的产量 |
下列叙述中能证明次氯酸是一种弱酸的是( )
| A、次氯酸不稳定,易分解 |
| B、次氯酸是一种强氧化剂 |
| C、次氯酸钙能与碳酸作用生成碳酸钙和次氯酸 |
| D、次氯酸能使染料和有机色质褪色 |
下列各组物质中,所含化学键类型完全相同的是( )
| A、HCl和MgCl2 |
| B、H2O和CO2 |
| C、Ar和CCl4 |
| D、NH4Cl和NaOH |
在15mL苯中溶解560mL乙炔,再加入75g苯乙烯,所得混和液中碳元素的质量分数为( )
| A、40% | B、66.7% |
| C、75% | D、92.3% |
化学与生产、生活、社会密切相关,下列说法正确的是( )
| A、煤经气化和液化两个物理过程后可变为清洁能源,这是煤综合利用的主要方法 |
| B、蛋白质、淀粉、纤维素、油脂等都能在人体内水解并提供能量 |
| C、利用风能发电、使用太阳能热水器、应用无氟制冷剂均有利于降低大气中的二氧化碳 |
| D、积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料 |
100mL浓度为2mol?L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是( )
| A、加入适量的6mol?L-1的盐酸 |
| B、加入适量的氯化钠溶液或降温 |
| C、加入适量CH3COOK溶液 |
| D、加入2滴氯化铜溶液或碳粉 |
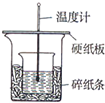 实验室利用如图装置进行中和热的测定,请回答下列问题:
实验室利用如图装置进行中和热的测定,请回答下列问题: