题目内容
【题目】已知:①2HI+Cl2=2HCl+I2,②2Fe+3Cl2=2FeCl3,③2FeBr2+3Cl2=2FeCl3+2Br2.在一定条件下HI、Fe、FeBr2分别与足量的Cl2反应,如果三个反应电子转移数目相等,则HI、Fe、FeBr2的物质的量之比为
A. 1:1:1 B. 1:3:3 C. 3:1:1 D. 6:3:2
【答案】C
【解析】
反应中只有氯气是氧化剂,3个反应得失电子数目相等,则3个反应中参加反应的氯气的物质的量相等,令参加反应的氯气为1mol,根据2HI+Cl2═2HCl+I2 ,n(HI)=2mol,根据2Fe +3Cl2═2FeCl3,n(Fe)=![]() mol,根据2FeBr2+3Cl2═2FeCl3+2Br2,n(FeBr2)=1mol×
mol,根据2FeBr2+3Cl2═2FeCl3+2Br2,n(FeBr2)=1mol×![]() =
=![]() mol,故n(HI):n(Fe):n(FeBr2)=2mol:
mol,故n(HI):n(Fe):n(FeBr2)=2mol:![]() mol:
mol:![]() mol=3:1:1,答案选C。
mol=3:1:1,答案选C。

【题目】根据题目要求回答下列问题:
(1)某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀,相同温度下,溶解度AgSCN>AgI。
操作步骤 | 现象 |
步骤1:向2 mL 0.005 mol/L AgNO3溶液中加入2 mL 0.005 mol/L KSCN溶液,静置 | 出现白色沉淀 |
步骤2:取1 mL上层清液于试管中,滴加1滴2 mol/L Fe(NO3)3溶液 | 溶液变为红色 |
步骤3:向步骤2的溶液中继续加入5滴3 mol/L AgNO3溶液 | 溶液浑浊、红色变浅 |
步骤4:向步骤1余下的浊液中加入5滴3 mol/L KI溶液 | 出现黄色沉淀 |
① 步骤3实验目的是_____________________________。
② 用化学平衡原理解释步骤4中的实验现象:___________________________。
(2)已知:
NH4Cl(s) = NH3(g) + HCl(g) ΔH = +163.9 kJmol-1
HCl(g) + CH3OH(g) = CH3Cl(g) + H2O(g) ΔH = -31.9 kJmol-1
①写出氯化铵和甲醇反应的热化学方程式____________________________,该反应在一定条件下能自发进行的原因是___________________________。
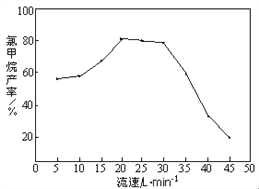
②由下图知,HCl和CH3OH的混合气体通过催化剂时的最佳流速在20 Lmin-1~30 Lmin-1之间。流速过快,会导致氯甲烷产率下降,原因是_________________________。流速过慢,会使副产物二甲醚增多,其反应为2CH3OH → CH3OCH3 + H2O,生产中常通入适量的水蒸气,该操作对制备CH3Cl的影响是___________________________。
(3)某高能锂离子电池充电时,总反应方程式为LiMn2O4=Li1-xMn2O4+xLi。则充电时阳极的电极反应方程式为______________________________________________。若电池的化学能转化为电能时的能量转化率为90%,则当消耗14 g锂时,电路中转移的电子数目为__________NA。