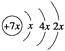题目内容
【题目】A、B、C、D都是短周期元素,原子半径:D>C>A>B。已知:A、B同周期,A、C处于同一主族;C原子核内的质子数等于A、B原子核内的质子数之和;C原子最外层电子数是D原子最外层电子数的3倍。试回答:
(1)写出元素的名称:A__________。
(2)写出由B、D组成的两种化合物的电子式分别为:___________、__________。
(3)A、C的最高价氧化物对应水化物中酸性较强的是__________(写水化物的分子式)。
(4)写出C的氧化物与D的最高价氧化物对应水化物反应的离子方程式_______________________。
【答案】硼 ![]()
![]() H3BO3 Al2O3+2OH-===2AlO2-+H2O
H3BO3 Al2O3+2OH-===2AlO2-+H2O
【解析】
根据原子半径D>C>A>B,且A、B同周期,A、C同主族,推知A、B、C、D在周期表中的大致相对位置为:,C的原子核内的质子数等于A、B原子核内的质子数之和,可知原子序数C=A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,故D为Na元素,C为Al元素,A为B元素,根据元素对应原子的结构判断元素在周期表中的位置,结合元素对应化合物的性质解答该题。
(1)元素A是B元素,名称为硼;
(2) B、D两元素可形成两种离子化合物,分别为Na2O、Na2O2,其阴、阳离子数之比均为1:2,电子式分别为:![]() 、
、![]() ;
;
(3)非金属性越强,最高价氧化物对应水化物中酸性越强。非金属性:B>Al,故最高价氧化物对应水化物中酸性较强的是H3BO3;
(4) Al2O3与NaOH溶液反应的离子方程式为Al2O3+2OH-===2AlO2-+H2O。

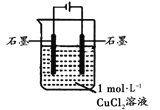
【题目】某小组同学利用下图装置对电解氯化铜实验进行了研究。
装置 | 现象 |
| 电解一段时间时,阳极石墨表面产生气体,阴极石墨上附着红色物质,溶液由蓝色变为绿色 |
(1)甲认为电解过程中阳极产生的_________是溶液变绿的原因,写出产生该物质的电极反应式:_________________________。
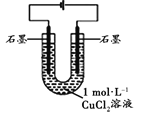
(2)乙改用下图装置,在相同条件下电解CuCl2溶液,对溶液变色现象继续探究。
装置 | 现象 |
| 电解相同时间时,阳极石墨表面产生气泡,溶液仍为蓝色;阴极石墨上附着红色物质,溶液由蓝色变为绿色; |
乙通过对现象分析证实了甲的观点不是溶液变绿的主要原因。乙否定甲的依据是______________。
(3)乙继续查阅资料:
i. 电解CuCl2溶液时可能产生[CuCl2]--,[CuCl2]- 掺杂Cu2+ 后呈黄色
ii. 稀释含[CuCl2]- 的溶液生成CuCl白色沉淀,据此乙认为:电解过程中,产生[CuCl2]_掺杂Cu2+后呈黄色,与CuCl2蓝色溶液混合呈绿色。
乙进行如下实验:
a.取电解后绿色溶液2 mL,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
b. 另取少量氯化铜晶体和铜粉,向其中加2 mL浓盐酸,加热获得含[CuCl2]_的黄色溶液。
c. 冷却后向上述溶液……
d. 取c中2 mL溶液,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
① a的目的是__________________________________________。
② 写出b中生成[CuCl2]- 的离子方程式:____________________________________________。
③ 补充c中必要的操作及现象:____________________________________________。
乙据此得出结论:电解时阴极附近生成[CuCl2]- 是导致溶液变绿的原因。