题目内容
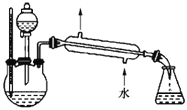
【题目】如图所示的实验装置可用来测定含两种元素的某种气体X的分子式。
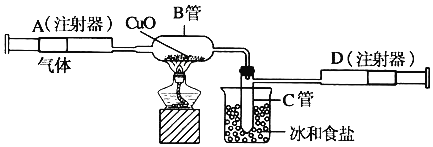
在注射器A中装有260毫升气体X并慢慢通过不含空气并装有红热的氧化铜的玻璃管B,使之完全反应,得到以下实验结果:实验前B管重![]() 克,实验后B管重
克,实验后B管重![]() 克,B管中的黑色粉末变成红色粉末。在C管中收集到的无色液体是水;在注射器D中收集到的气体是氮气。试回答下列问题:
克,B管中的黑色粉末变成红色粉末。在C管中收集到的无色液体是水;在注射器D中收集到的气体是氮气。试回答下列问题:
(1)X气体是由______和______元素组成的。
(2)若260毫升X气体完全反应后,收集到的氮气质量是0.28克。根据实验时温度和压强计算1摩尔X气体的体积是26000毫升,则X的摩尔质量是______克/摩尔。
(3)通过计算,确定X的分子式为______。
【答案】N H 32 ![]()
【解析】
(1)由题目信息可知,C管中收集到水,D中收集到N2,说明气体X与氧化铜反应有氮气、水生成,气体X只含有两种元素,根据元素守恒可知气体X含有的元素;
(2)1molX的气体的体积是26000mL,故260mLX气体的物质的量为0.01mol,反应收集到氮气的质量是0.28g,物质的量为0.01mol。B管中CuO含O:20.32 g-20.00 g=0.32 g,物质的量为0.02mol,故生成的水中H元素的质量为0.04mol×1g/mol=0.04g,所以气体X的质量为0.28g+0.04g=0.32g,再根据摩尔质量等于计算气体X的摩尔质量;
(3)根据(2)中可知气体X的物质的量,含有的N、H原子的物质的量,据此书写气体X的分子式。
![]() 管中收集到水,D中收集到
管中收集到水,D中收集到![]() ,说明气体X与氧化铜反应有氮气、水生成,气体X只含有两种元素,根据元素守恒可知,气体X含有N、H元素;
,说明气体X与氧化铜反应有氮气、水生成,气体X只含有两种元素,根据元素守恒可知,气体X含有N、H元素;
![]() 的气体的体积是24000mL,则260mLX气体的物质的量为:
的气体的体积是24000mL,则260mLX气体的物质的量为:![]() ,反应收集到氮气的质量是
,反应收集到氮气的质量是![]() ,物质的量为:
,物质的量为:![]() 。B管中CuO含O:
。B管中CuO含O:![]()
![]()
![]() g,物质的量为:
g,物质的量为:![]() ,
,![]() ,则生成的水中H元素的质量为:
,则生成的水中H元素的质量为:![]()
![]() ,所以气体X的质量为:
,所以气体X的质量为:![]() ,则气体X的摩尔质量为:
,则气体X的摩尔质量为:![]() ;
;
![]() 根据
根据![]() 中可知,
中可知,![]() mol,
mol,![]() ,
,![]()
![]() ,则
,则![]() :
:![]() :
:![]() mol:
mol:![]() mol:
mol:![]() :2:4,所以X的化学式为
:2:4,所以X的化学式为![]() 。
。