题目内容
下列电子式或结构式错误的是( )
A、OH-的电子式  |
B、NH4Br的电子式 |
C、CCl4的电子式  |
| D、H2O的结构式H-O-H |
考点:电子式,结构式
专题:化学用语专题
分析:A、无论是简单阴离子,还是复杂的阴离子,都应标出电子对等,还应加中括号,并在括号的右上方标出离子所带的电荷;
B、溴化铵是离子化合物,由铵根离子和溴离子构成,复杂的阳离子电子式除应标出共用电子对、非共用电子对等外,还应加中括号,并在括号的右上方标出离子所带的电荷;
C、氯原子未成键的孤对电子对未标出;
D、用短线“-”代替共用电子对即为结构式.
B、溴化铵是离子化合物,由铵根离子和溴离子构成,复杂的阳离子电子式除应标出共用电子对、非共用电子对等外,还应加中括号,并在括号的右上方标出离子所带的电荷;
C、氯原子未成键的孤对电子对未标出;
D、用短线“-”代替共用电子对即为结构式.
解答:
解:A、氧原子与氢原子以1对共用电子对连接,氢氧根是原子团阴离子,要用中括号括起来,并在右上角表明电荷数,故A正确;
B、溴化铵是离子化合物,由铵根离子和溴离子构成,电子式为 ,故B正确;
,故B正确;
C、氯原子未成键的孤对电子对未标出,四氯化碳电子式为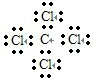 ,故C错误;
,故C错误;
D、H2O中氧原子与氢原子之间以1对共用电子对连接,电子式为 ,结构式为H-O-H,故D正确.
,结构式为H-O-H,故D正确.
故选C.
B、溴化铵是离子化合物,由铵根离子和溴离子构成,电子式为
 ,故B正确;
,故B正确;C、氯原子未成键的孤对电子对未标出,四氯化碳电子式为
 ,故C错误;
,故C错误;D、H2O中氧原子与氢原子之间以1对共用电子对连接,电子式为
 ,结构式为H-O-H,故D正确.
,结构式为H-O-H,故D正确.故选C.
点评:本题考查常用电子式与结构式的书写,难度不大,注意未成键的孤对电子对容易忽略.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
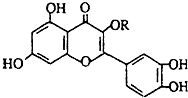 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )| A、1mol维生素P在一定条件下最多可以和7mol H2反应 |
| B、分子中共有两个苯环 |
| C、维生素P能与FeCl3溶液发生显色反应 |
| D、1mol维生素P可以和4mol NaOH反应 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、在水溶液中:H+、I-、NO3-、SiO32- |
| B、饱和氯水中:Cl-、NO3-、Na+、SO32- |
| C、酸性溶液中:H+、NH4+、Al3+、SO42- |
| D、碱性溶液中:NO3-、I-、Na+、Al3+ |
2013年11月29日,发生在山东圆通的夺命快递,导致1人死亡9人中毒.从物质的角度分析,是源于氟乙酸甲酯(FCH2COOCH3)中毒引起的.下列有关氟乙酸甲酯的说法不正确的是( )
| A、氟乙酸甲酯含有两种官能团 |
| B、1mol氟乙酸甲酯与NaOH水溶液共热最多消耗2mol NaOH |
| C、氟乙酸甲酯的同分异构体属于羧酸类的有2种 |
| D、氟乙酸甲酯加入稀硫酸共热后生成的有机物是HOCH2COOH和CH3OH |
室温下,pH=a的强酸与pH=b的强碱溶液等体积混合,混合后溶液中H+的物质的量浓度为4.5×10-3mol?L-1(混合前后体积变化不计),已知a+b=13,则a值为( )
| A、1 | B、2 | C、3 | D、4 |
下列有机实验操作或叙述正确的是( )
| A、将乙烯和乙炔气体分别通入溴的四氯化碳溶液中前者褪色,后者不褪色 |
| B、鉴别乙烷和乙炔可将二者分别通入酸性高锰酸钾溶液中 |
| C、苯能使溴水褪色是因为二者反应生成了溴苯 |
| D、工业上制备氯乙烯可用乙炔在一定条件下与氯化氢发生取代反应 |
如图,将纯铁棒和石墨棒插入1L饱和NaCl溶液中.下列说法正确的是( )


| A、将M、N用导线直接相连,在溶液中滴入酚酞溶液,石墨电极周围溶液变红 |
| B、M接电源正极,N接电源负极,当两极产生气体总量为22.4 mL(标准状况)时,则生成0.001 mol NaOH |
| C、M接电源正极,N接电源负极,将石墨电极换成Cu电极,电解质溶液换成CuSO4溶液,则可实现在铁上镀铜 |
| D、M接电源正极,N接电源负极,若把烧杯中溶液换成1 L CuSO4溶液,反应一段时间后,烧杯中产生蓝色沉淀 |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为( )
| A、氨气分子是极性分子而甲烷是非极性分子 |
| B、NH3分子中有一对未成键的弧对电子,它对成键电子的排斥作用较强 |
| C、NH3为分子中N原子形成3个杂化轨道,CH4中C原子形成4个杂化轨道 |
| D、两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化 |