题目内容
现有一定量的铁粉和铜粉的混合物,将其平均分成四等份,分别加入同浓度不同体积的稀硝酸,充分反应后,在标准状况下生成NO的体积和剩余金属的质量如下表(假设硝酸的还原产物只有NO一种):
根据上表中的数据计算分析,下列推断正确的是( )
A.①中溶解了5.6 g Fe B.②中溶解了9.6 g Cu
C.硝酸的浓度为4 mol/L D.④中V = 6720
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属/g | 18.0 | 9.6 | 0 | 0 |
| NO体积/mL | 2240 | 4480 | 6720 | V |
A.①中溶解了5.6 g Fe B.②中溶解了9.6 g Cu
C.硝酸的浓度为4 mol/L D.④中V = 6720
C
:由第一组数据可知固体有剩余.无论硝酸和什么金属反应,根据N原子守恒得,n(HNO3)="4" n(NO).
加入100 mL硝酸溶液时,n(NO)=0.1mol,则n(HNO3)=0.4mol,所以c(HNO3)=4mol/L.
故:c(HNO3)="4mol/L"
由1、2两组数据分析,两次剩余物的质量相差8.4g,此时生成2.24 LNO气体(转移0.3mol电子).
若只溶解铁,质量为8.4 g,若只溶解铜,质量为9.6 g.由此可知,当加入200ml硝酸溶液时,均溶解的是金属铁:
再由2、3两组数据分析,剩余的9.6g金属又恰好被等量的硝酸所溶解
综合可知,每份混合物中铁粉的质量为8.4×2=16.8g,即0.3mol;铜粉的质量为9.6g,即0.15mol;
④中,除了金属与硝酸生成的6720mlNO(0.3mol)气体外,溶液中的0.3mol的Fe2+也可被硝酸氧化,同时产生NO气体,由电子得失守恒可知NO为0.1mol,共0.4mol,8960ml
综上所述,答案为C
加入100 mL硝酸溶液时,n(NO)=0.1mol,则n(HNO3)=0.4mol,所以c(HNO3)=4mol/L.
故:c(HNO3)="4mol/L"
由1、2两组数据分析,两次剩余物的质量相差8.4g,此时生成2.24 LNO气体(转移0.3mol电子).
若只溶解铁,质量为8.4 g,若只溶解铜,质量为9.6 g.由此可知,当加入200ml硝酸溶液时,均溶解的是金属铁:
再由2、3两组数据分析,剩余的9.6g金属又恰好被等量的硝酸所溶解
综合可知,每份混合物中铁粉的质量为8.4×2=16.8g,即0.3mol;铜粉的质量为9.6g,即0.15mol;
④中,除了金属与硝酸生成的6720mlNO(0.3mol)气体外,溶液中的0.3mol的Fe2+也可被硝酸氧化,同时产生NO气体,由电子得失守恒可知NO为0.1mol,共0.4mol,8960ml
综上所述,答案为C

练习册系列答案
相关题目
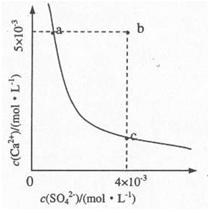
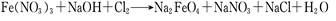
 的量浓度为 .
的量浓度为 .