题目内容
AD
稀释时电离程度增大,使c(H+)增大;但溶液体积增大,使c(H+)减小。若稀释时使离子数目增加优势于使溶液体积增加,则c(H+)增大;若稀释时体积增大占主要地位,虽离子绝对数增加,但c(H+)却减小。由于0.1 mol·L-1 CH3COOH属稀溶液,故加水稀释时,平衡右移,离子数增加,但主要是体积增大,c(H+)减小,所以A、D正确。?

练习册系列答案
相关题目
甲酸的下列性质中,可以证明它是弱电解质的是( )
| A.1mol·L-1的甲酸溶液的pH约为2 |
| B.甲酸能与水以任意比例互溶 |
| C.甲酸能使紫色石蕊试液变红 |
| D.在相同条件下,甲酸溶液的导电性比盐酸溶液的导电性弱 |
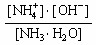 。氨水中各离子和分子的浓度大小关系为( )
。氨水中各离子和分子的浓度大小关系为( )