题目内容
X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的阴离子核外电子排布与氦原子相同,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍,M是地壳中含量最高的金属元素。下列说法中正确的是
| A.五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X |
| B.化合物X2W2、YW2、ZW2等都含有极性共价键和非极性共价键 |
| C.用M单质作阳极,石墨电极作阴极电解NaHCO3溶液,电解一段时间后,在阴极区会出现白色沉淀 |
| D.X、Z两元素能形成原子个数比为3∶1和4∶2的化合物 |
D
X元素为H、Y元素为C、M元素为Al;常见的气体单质有H2、N2、O2、F2、Cl2,所以Z、W分别为N、O;原子半径Al>C>N>O>H,可知A选项错误;CO2、NO2中只含极性共价键,B错误;阳极生成的Al3+与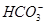 反应生成Al(OH)3沉淀,错误;由NH3、N2H4可知D选项正确。
反应生成Al(OH)3沉淀,错误;由NH3、N2H4可知D选项正确。
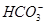 反应生成Al(OH)3沉淀,错误;由NH3、N2H4可知D选项正确。
反应生成Al(OH)3沉淀,错误;由NH3、N2H4可知D选项正确。
练习册系列答案
相关题目
 W合金(Z17W12)是一种潜在的贮氢材料,由Z、W单质在一定条件下熔炼而成。该合金在一定条件下完全吸氢的反应方程式为:Z17W12+17H2
W合金(Z17W12)是一种潜在的贮氢材料,由Z、W单质在一定条件下熔炼而成。该合金在一定条件下完全吸氢的反应方程式为:Z17W12+17H2 17ZH2+12W,得到的混合物Q(17ZH2+12W)在6.0 mol·L-1HCl溶液中能完全释放出H2。1 mol Z17W12完全吸氢后得到的混合物Q与上述盐酸完全反应,释放出H2的物质的量为 。
17ZH2+12W,得到的混合物Q(17ZH2+12W)在6.0 mol·L-1HCl溶液中能完全释放出H2。1 mol Z17W12完全吸氢后得到的混合物Q与上述盐酸完全反应,释放出H2的物质的量为 。 ,则该元素在周期表中位于第三周期、ⅥA族
,则该元素在周期表中位于第三周期、ⅥA族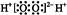
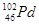 和
和 互为同位素
互为同位素 2H2O+O2↑和 。若在X极收集气体672 mL,在Y极收集气体168 mL(均已折算为标况下体积),则Y电极质量减少 g。
2H2O+O2↑和 。若在X极收集气体672 mL,在Y极收集气体168 mL(均已折算为标况下体积),则Y电极质量减少 g。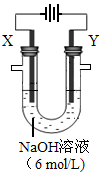
 2SO3(g) △H<0,其它条件不变时加入催化剂,反应速率v(SO2)和SO2转化率均增大
2SO3(g) △H<0,其它条件不变时加入催化剂,反应速率v(SO2)和SO2转化率均增大