题目内容
【题目】次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式:_______________________________________
(2)(H3PO2)中,磷元素的化合价为_________________
(3)H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银。利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:________填化学式)
(4)已知:甲醇脱水反应 ①2CH3OH(g)=CH3OCH3(g)+H2O(g) △H1=-23.9kJ·mol-1
甲醇制烯烃反应
②2CH3OH(g)=C2H4 (g)+2H2O(g) △H2=-29.1kJ·mol-1
乙醇异构化反应
③CH3CH2OH(g)=CH3OCH3(g)) △H3=+50.7kJ·mol-1
则乙烯气相直接水合反应C2H4 (g)+H2O(g)=C2H5OH(g)的 △H=________kJ·mol-1
(5)下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系[(其中n(H2O)︰n(C2H4)=1︰1]

①列式计算乙烯水合制乙醇反应在图中A点的平衡常数K=________________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
②图中压强P1、P2、P3、P4的大小顺序为:______,理由是:__________
【答案】 H3PO2 ![]() H++H2PO2- +1 H3PO4 -45.5 K=0.07(MPa)-1 P1< P2< P3< P4 反应分子数减少,相同温度下,压强升高,乙烯转化率提高
H++H2PO2- +1 H3PO4 -45.5 K=0.07(MPa)-1 P1< P2< P3< P4 反应分子数减少,相同温度下,压强升高,乙烯转化率提高
【解析】(1)H3PO2是一元中强酸,溶液中部分电离出氢离子,所以其电离方程式为H3PO2![]() H2PO2-+H+;(2)H3PO2中,总化合价为0,其中氢元素为+1价,氧元素为-2价,则P元素的化合价为+1价;(3)该反应中Ag+为氧化剂,H3PO2为还原剂,氧化剂与还原剂的物质的量之比为4:1。设反应产物中P的化合价为x,根据化合价升降相等可得,4×(1-0)=1×(x-1),解得x=5,所以氧化产物为+5价的H3PO4;(4)已知:
H2PO2-+H+;(2)H3PO2中,总化合价为0,其中氢元素为+1价,氧元素为-2价,则P元素的化合价为+1价;(3)该反应中Ag+为氧化剂,H3PO2为还原剂,氧化剂与还原剂的物质的量之比为4:1。设反应产物中P的化合价为x,根据化合价升降相等可得,4×(1-0)=1×(x-1),解得x=5,所以氧化产物为+5价的H3PO4;(4)已知:
①2CH3OH(g)=CH3OCH3(g)+H2O(g) △H1=-23.9kJ·mol-1
②2CH3OH(g)=C2H4 (g)+2H2O(g) △H2=-29.1kJ·mol-1
③CH3CH2OH(g)=CH3OCH3(g)) △H3=+50.7kJ·mol-1
根据盖斯定律可知①-②-③即得到乙烯气相直接水合反应C2H4 (g)+H2O(g)=C2H5OH(g) 的反应热△H=-45.5 kJ·mol-1。
(5)①该温度下,乙烯的转化率为0.2,设起始时乙烯和水的物质的量为nmol,则反应的乙烯和水的物质的量分别为0.2nmol,平衡时两者的物质的量均为0.8nmol;生成的乙醇的物质的量为0.2nmol,平衡时总的物质的量为1.8nmol,乙烯、水、乙醇的物质的量分数分别为0.8/1.8,0.8/1.8,0.2/1.8,因此乙烯水合制乙醇反应在图中A点的平衡常数为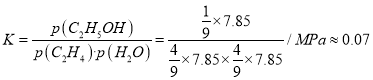 (MPa)-1;②由方程式C2H4 (g) + H2O(g)=C2H5OH(g)可知该反应的正反应是气体体积减小的反应,所以增大压强,平衡正向移动,乙烯的转化率提高,因此压强关系是:P1< P2< P3< P4。
(MPa)-1;②由方程式C2H4 (g) + H2O(g)=C2H5OH(g)可知该反应的正反应是气体体积减小的反应,所以增大压强,平衡正向移动,乙烯的转化率提高,因此压强关系是:P1< P2< P3< P4。

 名校课堂系列答案
名校课堂系列答案
