题目内容
下列有关说法正确的是( )
分析:A.作原电池负极的金属易被腐蚀,作正极的金属被保护;
B.反应热与反应物和生成物能量的相对大小有关;
C.无论反应是放热反应还是吸热反应,升高温度都加快反应速率;
D.氧化铝能保护铝不受腐蚀.
B.反应热与反应物和生成物能量的相对大小有关;
C.无论反应是放热反应还是吸热反应,升高温度都加快反应速率;
D.氧化铝能保护铝不受腐蚀.
解答:解:A.铜、铁和电解质溶液构成原电池,铁作负极而加速被腐蚀,铁、锌和电解质溶液构成的原电池中,铁作正极被保护,故A正确;
B.反应热与反应物和生成物能量的相对大小有关,所以CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,不能说明该反应的△H<0,故B错误;
C.无论反应是放热反应还是吸热反应,升高温度都加快反应速率,所以N2(g)+3H2(g)?2NH3(g)△H<0在其他条件不变时升高温度,反应速率V(H2)增大,故C错误;
D.铝是亲氧元素,铝的表面生成一层致密的氧化物薄膜而阻止铝被腐蚀,故D错误;
故选A.
B.反应热与反应物和生成物能量的相对大小有关,所以CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,不能说明该反应的△H<0,故B错误;
C.无论反应是放热反应还是吸热反应,升高温度都加快反应速率,所以N2(g)+3H2(g)?2NH3(g)△H<0在其他条件不变时升高温度,反应速率V(H2)增大,故C错误;
D.铝是亲氧元素,铝的表面生成一层致密的氧化物薄膜而阻止铝被腐蚀,故D错误;
故选A.
点评:本题考查较综合,涉及原电池原理、反应热、反应速率的影响因素等知识点,易错选项是C,注意无论反应是放热反应还是吸热反应,升高温度都加快反应速率,但平衡向吸热反应方向移动,为易错点.

练习册系列答案
相关题目
 (2012?绵阳模拟)钾在氧气中燃烧时得到一种钾的氧化物晶体,其结构如图所示,下列有关说法正确的是( )
(2012?绵阳模拟)钾在氧气中燃烧时得到一种钾的氧化物晶体,其结构如图所示,下列有关说法正确的是( )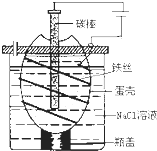 工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,
工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,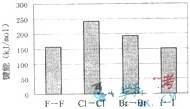 (2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.