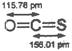
题目内容
【化学选修5:有机化学基础】
PET是世界上产量最大的合成纤维,其结构简式为:
现以煤的干馏产品A与F为原料制备PET,生产流程如下图所示。其中A为烃,含碳元素的质量分数为90.6%,其蒸气的密度是空气密度的3.66倍,能使酸性高锰酸钾溶液褪色,但不能使溴水褪色。M分子里所有原子共平面。
请回答下列问题:
(1)指出下列反应类型:④ ⑤
(2)指出反应①的反应条件:
(3)写出有机物的结构简式,A: ;N: 。
(4)写出下列反应的化学方程式:
反应② 反应③ 反应⑤
(5)P的一种同系物X分子式为C3H8O2,在核磁共振氢谱图中出现三种信号峰,其峰的强度之比为2︰1︰1。则X的结构简式为 。
(1)加成反应 缩聚反应(各1分)
(2)NaOH的水溶液加热(或强碱水溶液加热)(1分)
(3) (各2分)
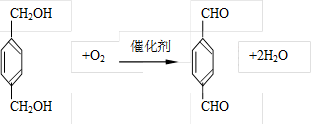 (4)(方程式各2分)
(4)(方程式各2分)
②
③CaC2+2H2O→Ca(OH)2+HC≡CH↑
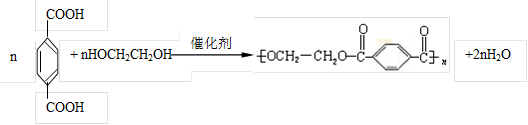 ⑤
⑤
(5)
解析:

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案
相关题目