题目内容
分析某种煤气的体积组成如下:H2 50%、CH4 30%、CO 10%、N2 6%、CO2 4%。已知:H2(g)+![]() O2(g)====H2O(l);ΔH=-285.8 kJ·mol-1
O2(g)====H2O(l);ΔH=-285.8 kJ·mol-1
CO(g)+![]() O2(g)====CO2(g);ΔH=-282.6 kJ·mol-1
O2(g)====CO2(g);ΔH=-282.6 kJ·mol-1
CH4(g)+2O2(g)====CO2(g)+2H2O(l);ΔH=-890.3 kJ·mol-1
则在标准状况下,224 L该种煤气燃烧时放出的热量为( )
A.1461.7 kJ B.4382.5 kJ C.4665.1 kJ D.5811.5 kJ
B
解析:本题考查热化学方程式的计算。由题意知224 L该种煤气中含H2:(224 L×50%)÷22.4 L·mol-1=5 mol,完成燃烧放出热量为5 mol ×285.8 kJ·mol-1=1429 kJ;同理CO放热(224 L×10%)÷22.4 L·mol-1×282.6 kJ·mol-1=282.6 kJ;CH4放热(224 L×30%)÷22.4 L·mol-1×890.36 kJ·mol-1=2670.9 kJ。三者热量之和为4382.5 kJ,B正确。

 名校课堂系列答案
名校课堂系列答案Ⅰ.实验表明,CuO被H2还原时也有Cu2O生成。将一定量的H2缓慢通过灼热的CuO粉末,得到固体混合物且混合物中m(Cu)∶m(O)=8∶a。当a有不同的取值时,固体混合物成分不同。请分析a的取值范围和固体混合物成分的关系并填入下表(不一定填满,表格不够也可自行增加)。
a的取值范围 | 反应后固体的成分(用化学式表示) |
|
|
|
|
|
|
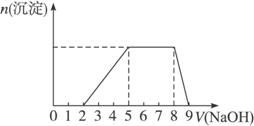
Ⅱ.黄铜矿的主要成分X是由Cu、Fe、S三种元素组成的复盐,其中Cu、Fe两种元素的质量比为8∶7;将m g X粉末全部溶于200 mL的浓HNO3,反应后的溶液加水稀释至2.12 L时测得其pH为0;将稀释后的溶液分为两等份,向其中一份溶液中滴加6.05 mol·L-1的NaOH溶液,向另一份溶液中滴加0.600 mol·L-1 Ba(NO3)2溶液,两溶液中均生成沉淀,且沉淀的质量随所加溶液的体积变化如下图所示:
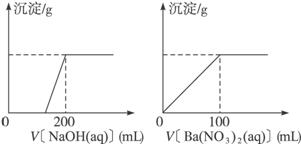
(1)请通过计算确定m的值;
(2)X的摩尔质量为368 g·mol-1,请确定X的化学式_______________