题目内容
Ⅰ.某溶液中可能含有H+、Na+、
Ⅱ.已知X、Y、Z、W是短周期中的四种非金属元素,它们的原子序数依次增大。X元素原子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍。
(1)仅由X、Z、W三种元素组成的某种盐是一种速效肥料,但长期施用会使土壤酸化,有关的离子方程式为:____________。
(2)这四种元素可组成原子个数比为5∶1∶1∶3的化合物(按X、Y、Z、W的顺序),该化合物的水溶液与足量的NaOH溶液反应的离子方程式为____________。
(3)将9 g Y单质在足量W单质中燃烧。所得气体通入1 L 1 mol·L-1的NaOH溶液中,完全吸收后,溶液中的离子浓度由大到小的顺序是____________。
Ⅰ.H+、![]() 、Al3+ 2∶3∶1 Fe3+、Mg2+
、Al3+ 2∶3∶1 Fe3+、Mg2+
Ⅱ.(1) ![]() +H2O
+H2O![]() NH3·H2O+H+
NH3·H2O+H+
(2) ![]() +
+![]() +2OH-
+2OH-![]() NH3↑+2H2O+
NH3↑+2H2O+![]()
(3)c(Na+)>c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
解析:Ⅰ.由0—2无沉淀可知含H+2份。

由2—5产生沉淀及8—9沉淀恰好溶解可知消耗三份NaOH生成沉淀,消耗一份NaOH沉淀恰好溶解。则含Al3+为1份。
5—8沉淀无变化则含![]() 为3份。
为3份。
即H+、![]() 、Al3+物质的量之比2∶3∶1,不含Fe3+、Mg2+。
、Al3+物质的量之比2∶3∶1,不含Fe3+、Mg2+。
Ⅱ.据题意,可推知X—H、Y—C、Z—N、W—O
(1)速效肥料为NH4NO3,长期使用能使土壤酸化
有关离子方程式:![]() +H2O
+H2O![]() NH3·H2O+H+
NH3·H2O+H+
(2)原子个数比为H∶C∶N∶O=5∶1∶1∶3,即NH4HCO3,该化合物的水溶液与足量的NaOH溶液反应的离子方程式![]() +
+![]() +2OH-====NH3↑+2H2O+
+2OH-====NH3↑+2H2O+![]()
(3)将9 g碳在足量的O2中燃烧生成0.75 mol CO2,通入1 L 1 mol·L-1NaOH溶液中完全吸收,设生成Na2CO3、NaHCO3的物质的量分别为x、y,![]()
![]()
即含0.25 mol Na2CO3、0.5 mol NaHCO3的溶液中离子浓度之比c(Na+)>c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+)。
)>c(OH-)>c(H+)。

 名校课堂系列答案
名校课堂系列答案| A、肯定不含I- | B、肯定不含NH+4 | C、可能含有SO2-3 | D、可能含有I- |
| A、一定含有Mg2+、Al3+、Clˉ,不含Na+、NH4+ | B、一定含有Na+、Mg2+、Clˉ,不含NH4+,可能含有Al3+ | C、c (Clˉ) 为 4.00 mol?L-1,c (Al3+) 为1.00 mol?L-1 | D、c (Mg2+) 为 1.00 mol?L-1,c(Na+) 为 1.50 mol?L-1 |
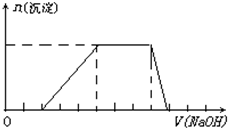 某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液体积的变化如图所示,由此可知,该溶液中一定含有的阳离子是
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液体积的变化如图所示,由此可知,该溶液中一定含有的阳离子是