题目内容
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成: ① 与
与 ②
② 与NaOH ③
与NaOH ③ 与
与 ④
④ 与
与 ,下列各项排序正确的是
,下列各项排序正确的是
 与
与 ②
② 与NaOH ③
与NaOH ③ 与
与 ④
④ 与
与 ,下列各项排序正确的是
,下列各项排序正确的是| A.pH:②>③>④>① | B. :②>④>③>① :②>④>③>① |
| C.溶液中c(H+): ①>③>②>④ | D. : ①>④>③>② : ①>④>③>② |
B
试题分析:A.这几组混合物中都含有醋酸钠,盐酸溶液呈酸性,氢氧化钠溶液呈强碱性,氯化钠溶液呈中性,碳酸氢钠溶液呈弱碱性,所以这几种溶液pH大小顺序是②>④>③>①,故A错误;B.盐酸抑制醋酸根离子水解,氢氧化钠抑制醋酸根离子水解,氯化钠既不抑制也不促进醋酸根离子水解,碳酸氢根离子抑制醋酸根离子水解,但抑制能力小于氢氧根离子,所以溶液中醋酸根离子浓度大小顺序是②>④>③>①,故B正确;C.根据A知,这几种溶液中氢离子浓度大小顺序是②<④<③<①,故C错误;D.根据B知,醋酸根离子浓度越大,根据物料守恒知,醋酸分子的浓度就越小,所以醋酸分子浓度大小顺序是②<④<③<①,故D错误;故选:B.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
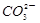 )=c(H+)+c(H2CO3)
)=c(H+)+c(H2CO3)