题目内容
【题目】锌锰碱性干电池是依据原电池原理制成的化学电源。电池中负极与电解质溶液接触直接反应会降低电池的能量转化效率,称为自放电现象。
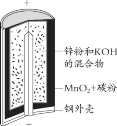

下列关于原电池和干电池的说法不正确的是
A. 两者正极材料不同
B. MnO2的放电产物可能是KMnO4
C. 两者负极反应式均为Zn失电子
D. 原电池中Zn与稀H2SO4存在自放电现象
【答案】B
【解析】
A、左图为干电池,干电池的正极材料是碳棒,右图为原电池,正极材料是铜单质,两者正极材料不同,故A说法正确;
B、干电池中MnO2应作氧化剂,Mn的化合价降低,故B说法错误;
C、所给装置中Zn为负极,Zn失去电子,故C说法正确;
D、根据自放电现象的定义,Zn与稀硫酸能够发生反应,即原电池中Zn与稀硫酸存在自放电现象,故D说法正确。

练习册系列答案
相关题目
【题目】在一体积固定的密闭容器中加入反应物A、B,发生如下反应:A(g)+2B(g) ![]() 3C(g)。反应过程中的部分数据如下表所示,下列说法正确的是
3C(g)。反应过程中的部分数据如下表所示,下列说法正确的是
浓度/ mol·Lˉ1 时间/min | c(A) | c(B) | c(C) |
0 | 1.0 | 1.2 | 0 |
2 | 0.8 | ||
4 | 0.6 | ||
6 | 0.9 |
A.0~2 min内,B的反应速率为0.1 mol·Lˉ1·minˉ1
B.2 min时,C的物质的量浓度为0.4 mol·Lˉ1
C.4 min时,反应已达到平衡状态,此时正、逆反应的速率都为0
D.4~6 min内,容器内气体分子的总物质的量不变