题目内容
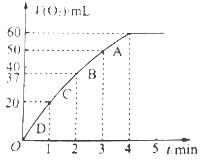
(共10分)某温度时,在2 L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示:
由图中数据分析求:
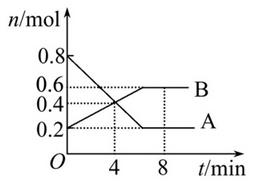
(1)该反应的化学方程式为 。(2分)
(2)反应开始 至4 min时,A的平均反应速率为 。(要求写出计算过程)(2分)
至4 min时,A的平均反应速率为 。(要求写出计算过程)(2分)
(3)第4min末时A、B的物质的量浓度依次为________(1分)、________(1分)。第4 min时,正、逆反应速率的大小关系为:v(正)________v(逆)(填“>”、“<”或“=”,下同)(2分),第8 min时,v(正)________v(逆)(2分)。
由图中数据分析求:

(1)该反应的化学方程式为 。(2分)
(2)反应开始
 至4 min时,A的平均反应速率为 。(要求写出计算过程)(2分)
至4 min时,A的平均反应速率为 。(要求写出计算过程)(2分)(3)第4min末时A、B的物质的量浓度依次为________(1分)、________(1分)。第4 min时,正、逆反应速率的大小关系为:v(正)________v(逆)(填“>”、“<”或“=”,下同)(2分),第8 min时,v(正)________v(逆)(2分)。
(共10分)(1)(2分)3A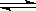 2B
2B
(2)(2分)0.05mol/(L· min)
(1分)0.2mol/L、(1分)0.2mol/L;(2分)> ,(2分)=
 2B
2B(2)(2分)0.05mol/(L· min)
(1分)0.2mol/L、(1分)0.2mol/L;(2分)> ,(2分)=
略

练习册系列答案
相关题目
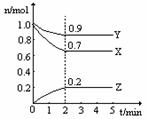
 2Z; 0.05 mol/(L·min)
2Z; 0.05 mol/(L·min)  2NH3),根据下列在相同时间内测定的正反应速率判断,生成NH3的速率最快的是
2NH3),根据下列在相同时间内测定的正反应速率判断,生成NH3的速率最快的是 

 ;经 2 s后测得 C 的物质的量浓度为 0.6 mol·L-1,现有下列几种说法:
;经 2 s后测得 C 的物质的量浓度为 0.6 mol·L-1,现有下列几种说法: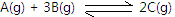 达到限度的是
达到限度的是 CO(g)+H2(g) ΔH=" +131.3" kJ?mol-1,
CO(g)+H2(g) ΔH=" +131.3" kJ?mol-1,  ”与“不能”);
”与“不能”); .c(CO)=c(H2) d.密闭容器的容积不再改变
.c(CO)=c(H2) d.密闭容器的容积不再改变