题目内容
下列有关叙述中,错误的是( )
| A.金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 |
| B.白磷分子晶体中,微粒之间通过共价键结合 |
| C.σ键可以单独存在,π键不可单独存在 |
| D.H2O的分解温度及沸点都比H2S高得多的事实不可都用氢键知识解释 |
B
试题分析:A.在金刚石中每个C原子以四个共价键与相邻的四个C原子相连,键角为109°28′。这种结构向空间扩展就形成了一种立体的网状结构。由共价键形成的最小碳环上含有6个碳原子。正确。B.白磷是由分子构成的分子晶体。在分子内,原子间以共价键结合。在分子间以分子间作用力结合。因此白磷是有白磷分子通过分子间作用力结合而成的分子晶体。错误。C.两个原子形成的共价键,可以只形成σ键,而不形成π键,但是只有形成π键,则一定同时还形成了σ键。因此σ键可以单独存在,π键不可单独存在。正确。D.氢键属于分子间作用力。而物质分解断裂的是化学键,因此不可用氢键知识解释。正确。

练习册系列答案
相关题目

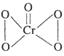 ,据此推断该氧化物
,据此推断该氧化物