��Ŀ����
����Ŀ���������仯��������������������Ҫ��Ӧ�á�
��1������O2��HClת��ΪCl2��4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)����֪��ػ�ѧ���ļ������±���ʾ
��ѧ�� | H-Cl | O=O | Cl �C Cl | H-O |
E(kJ��mol-1 | a | b | c | d |
��÷�Ӧ����H=______________��(�ú�a��b��c��d�Ĵ���ʽ��ʾ)
��2���������л��ϳ��е���Ҫ�Լ�����ϩ(CH2=CHCH3)��Cl2��һ�������·������·�Ӧ�� CH2=CHCH3 (g)+Cl2(g) ![]() CH2=CHCH2Cl(g)+HCl(g)��һ��ѹǿ�£��÷�Ӧ�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�ʱ����ƽ��ʱCl2��ת������ͼ��ʾ(T12< T3)
CH2=CHCH2Cl(g)+HCl(g)��һ��ѹǿ�£��÷�Ӧ�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�ʱ����ƽ��ʱCl2��ת������ͼ��ʾ(T12< T3)
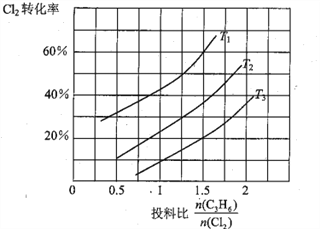
�ٸ÷�Ӧ����H______________0(����>������<��)
�����д�ʩ�������ϩ��ƽ��ת���ʵ���______________ (����)��
A.�����¶� B.��С���������
C.ʹ�����ʹ��� D.�������������Ȼ���
��T1ʱ�����ݻ�Ϊ5L���ܱ������г���0.15mol��ϩ��0.10 molCl2��10minʱ�ﵽƽ�⣬��v(Cl2)Ϊ______________mol����L��min)-1��ƽ�ⳣ��KΪ______________�������¶Ȳ��䣬��СͶ�ϱ�![]() ��Kֵ��______________ (��������������С������������)������ʼʱ��������г���0.30mol��ϩ��0.20 molCl2��0.15 mol CH2=CHCH2Cl��0.30 molHCl���жϷ�Ӧ���еķ���˵������____________________________��
��Kֵ��______________ (��������������С������������)������ʼʱ��������г���0.30mol��ϩ��0.20 molCl2��0.15 mol CH2=CHCH2Cl��0.30 molHCl���жϷ�Ӧ���еķ���˵������____________________________��
��������Ӧ�ڵ���ij�¶�ʱ��CH2=CHCH2Cl�IJ��ʿ����½������ܵ�ԭ����____________________________��
���𰸡� (4a+b-2c-4d) kJ/mol < AD 0.0012mol/(L��min) 1 ���� ������Ӧ�����������ΪQc=0.75��������) ��ϩ�����������˼ӳɷ�Ӧ (��������)
����������1�����鷴Ӧ�ȵļ��㣬��H=��Ӧ������ܺͣ�����������ܺ�=(4a��b��2c��4d)kJ��mol��1����2��������������ԭ������ѧ��Ӧ���ʼ��㡢��ѧƽ��ļ��㣬�ٸ���ͼ�������¶����ߣ�Cl2��ת���ʽ��ͣ�˵�������¶�ƽ�����淴Ӧ�����ƶ���������Ӧ��H<0����A������Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ�����ϩת��������A��ȷ��B����Ӧǰ������ϵ��֮����ȣ���С������������൱����ѹǿ��ƽ�ⲻ�ƶ�����B����C��ʹ�ô����Ի�ѧƽ���ƶ���Ӱ�죬��C����D�������Ȼ��⣬ƽ��������Ӧ�����ƶ�����ϩ��ת��������D��ȷ���۱�ϩ������Ͷ�ϱ�Ϊ0.15��0.10=1.5��T1��ʱ������ת����Ϊ60%��CH2=CHCH3 (g)+Cl2(g) ![]() CH2=CHCH2Cl(g)+HCl(g)
CH2=CHCH2Cl(g)+HCl(g)
��ʼ�� 0.15 0.1 0 0
�仯�� 0.06 0.06 0.06 0.06
ƽ�⣺ 0.09 0.04 0.06 0.06�����ݻ�ѧ��Ӧ������ѧ����ʽ��v(Cl2)=0.06/(5��10)mol/(L��min)=0.0012mol/(L��min)�����ݻ�ѧƽ�ⳣ���Ķ��壺K=1��Kֵֻ���¶ȵ�Ӱ�죬��СͶ�ϱȣ���ѧƽ�ⳣ�����䣬��ʱ��Ũ����Ϊ0.3��0.15/(0.3��0.2)=0.75<1���Ƴ���Ӧ������Ӧ������У��ܱ�ϩ�����������ӳɷ�Ӧ����ɲ��ʽ��͡�

����Ŀ������ͼ��ʾ��һЩ���ʻ�����Ĵ�����ϵ����ȷ����
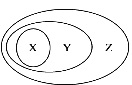
X | Y | Z | |
A | ˮ | ���� | ������ |
B | �ǽ��������� | ���������� | ������ |
C | ����� | ������ | ������ |
D | ���Ϸ�Ӧ | ������ԭ��Ӧ | ��ѧ��Ӧ |
A. A B. B C. C D. D