题目内容
下列有关说法正确的是
| A.同主族元素的原子序数可能相差16、26、36、50 |
| B.由两种不同原子组成的纯净物一定是化合物 |
| C.任何物质中都含有化学键,有化学键断裂的变化不一定属于化学变化 |
| D.镁、铝、铜、铁、钠五种金属元素中,铜和铁属于副族元素 |
A
试题分析:周期表中含有7个周期,含有的元素种类应该是2、8、8、18、18、32、32(排满),所以同主族元素的原子序数可能相差16、26、36、50,A正确。由两种不同原子组成的纯净物不一定是化合物,也可能是是单质,B不正确;稀有气体分子中不存在化学键,C不正确;铁是第Ⅷ族元素,D不正确,答案选A。
点评:该题是高考中的常见考点,属于中等难度试题的考查,试题基础性强,侧重对学生基础知识的巩固和训练,有利于培养学生的逻辑推理能力和发散思维能力,提高学生灵活运用基础知识解决实际问题的能力。

练习册系列答案
相关题目
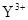 与
与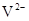 的核外电子数相等
的核外电子数相等