题目内容
【题目】图甲是H2O2酶活性受pH影响的曲线,图乙表示在最适温度下、pH=b时H2O2分解产生的O2量随时间的变化.若该酶促反应过程中改变某一初始条件,以下改变正确的是( )
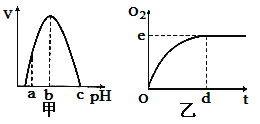
A.pH=a时,e点下移,d点左移
B.H2O2酶量增加时,e点上移,d点左移
C.H2O2量增加时,e点不移,d点左移
D.温度升高时,e点不移,d点右移
【答案】D
【解析】
试题O2的最大释放量只与H2O2的量有关,与酶的活性无关。与pH=b时相比,pH=a时酶的活性下降,e点不移,d点右移,A项错误;H2O2酶增加时,因H2O2量没有改变,所以e点不移,d点左移,B项错误;增加H2O2量,e点上移,d点右移,C项错误;温度升高时酶的活性降低,e点不移,但H2O2完全分解所用的时间延长,d点右移, D项正确。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】
Ⅰ.形式一:(由粒子数推断)![]() 、
、![]() 、
、![]() 、D、E 5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①
、D、E 5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①![]() ;②
;②![]() 。据此,回答下列问题:写出
。据此,回答下列问题:写出![]() 、
、![]() 的化学式:____、______、
的化学式:____、______、
Ⅱ. 形式二:(由元素原子结构推断)A、B、C、D、E、F的原子序数依次增大,它们都是同周期的元素。已知:A、C、F 三种原子最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多2。
(1)写出下列元素的符号:A________,B________,E________
(2)F在元素周期表中的位置为___________________________________
(3)写出C的单质和A的最高价氧化物的水化物反应的离子方程式_______
(4)元素的非金属性为(原子的得电子能力):E________F(填“强于”或“弱于”),请以E、F为例列举元素非金属性强弱的比较方法__________________________________________________(至少2条)
通过Ⅱ的解题你认为推断出本题各元素的关键环节为___________
III.形式三:(由元素位置推断)下表为元素周期表的一部分:
族 周期 | ||||||||
1 | ① | |||||||
2 | ② | |||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)请画出元素⑦的离子结构示意图________________。
(2)写出元素⑤在周期表中的位置______________。
(3)②、③、⑥的离子半径由大到小的顺序为_________________________。
(4)⑤、⑥、⑦的最高价氧化物对应水化物酸性由强到弱的顺序是______。
(5)①、②、③三种元素可形成既含离子键又含极性共价键的化合物,写出该化合物的电子式:____________________。该化合物与④的最高价氧化物反应的离子方程式为____________________。
(6)请你预测:如果发现了原子序数为116号元素,它在周期表中的位置是第________周期_______族,它属于_____元素(填“金属”或“非金属”)
【题目】某强酸性无色溶液中可能含下表中的若干种离子。
阳离子 | Mg2+、NH4+、Ba2+、Al3+、Fe2+ |
阴离子 | SiO32-、MnO4-、Cl-、NO3-、SO32-、 |
实验Ⅰ:取少量该试液进行如下实验。
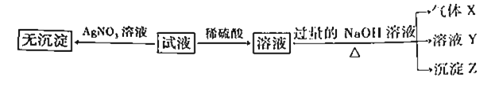
实验Ⅱ:为了进一步确定该溶液的组成,取100mL原溶液,向该溶液中滴加1mol·L-1的NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。

回答下列问题:
(1)不进行实验就可以推断出,上表中的离子一定不存在的有____________种。
(2)通过实验Ⅰ可以确定该溶液中一定存在的阴离子是________________。
(3)写出实验Ⅱ的图像中BC段对应的离子方程式:_______________________________________________________________。
(4)A点对应的固体质量为____________g。
(5)该溶液中阴离子的浓度为____________mol·L-1



