题目内容
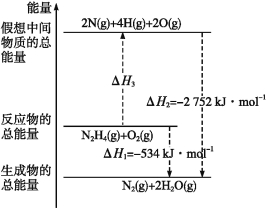
【题目】肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O![]() O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是
O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是
A.194 B.391 C.516 D.658
【答案】B
【解析】利用图示可知肼和氧气变成原子时断键需要的能量为2752 kJ-534 kJ=2218 kJ。1 mol肼和1 mol氧气断键变为原子时要断裂1 mol N—N,4 mol N—H,1 mol O![]() O键,所以1 mol×154 kJ·mol-1+4 mol×(N—H键的键能)+1 mol×500 kJ·mol-1=2218 kJ,解得N—H键的键能为391 kJ·mol-1,所以断裂1 mol N—H键所需的能量是391 kJ,选B。
O键,所以1 mol×154 kJ·mol-1+4 mol×(N—H键的键能)+1 mol×500 kJ·mol-1=2218 kJ,解得N—H键的键能为391 kJ·mol-1,所以断裂1 mol N—H键所需的能量是391 kJ,选B。

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目