题目内容
【题目】RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。如图为RFC工作原理示意图,下列有关说法正确的是
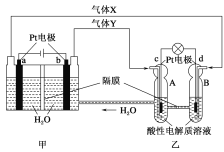
A. 图甲把化学能转化为电能,图乙把电能转化为化学能,水得到了循环使用
B. 当有0.1 mol电子转移时,a极产生0.56 L O2(标准状况下)
C. c极上发生的电极反应为O2+4H++4e-===2H2O
D. 图乙中电子从c极流向d极,提供电能
【答案】C
【解析】
根据图示知,图甲有外接电源,所以为电解池,a为电解池阴极,b为阳极,用惰性电极电解水时,阴极上氢离子放电生成氢气,阳极上氢氧根离子放电生成氧气;
图乙没有外接电源,属于原电池,c电极上氧气得电子发生还原反应,则为原电池正极,d电极上氢气失电子发生氧化反应而作原电池负极,电子从负极流向正极;
结合转移电子和气体之间的关系式进行计算来解答。
A.图甲有外接电源,所以该装置是将电能转化为化学能的装置,属于电解池,图乙能自发进行氧化还原反应,是将化学能转化为电能的装置,为原电池,选项A错误;
B.a电极作电解池阴极,阴极上氢离子放电生成氢气,选项B错误;
C.c电极上氧气得电子和氢离子反应生成水,电极反应式为O2+4H++4e-═2H2O,选项C正确;
D.图乙中c是正极,d是负极,电子从负极d流向正极c,选项D错误;
答案选C。

 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案【题目】(题文)根据物质结构有关性质和特点,回答以下问题:
(1)过渡元素Co 基态原子价电子轨道表达式为_______________________________。第四电离能I4 (Co) < I4 (Fe) ,其原因是__________________________________________。
(2)磷的氯化物有两种:PCl3和PCl5 ,PCl3中磷原子的杂化类型为__________,PCl3的立体构型为__________,其中PCl3的沸点________(填“大于”或“小于”)PCl5,原因是__________。
(3)酞菁铟是有机分子酞菁与金属铟形成的复杂分子,结构简式如下图所示,该分子中存在的化学键为___________(填选项字母)
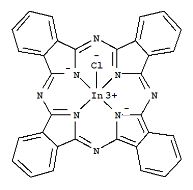
a.σ键 b.π键 c.离子键 d.配位键
(4)氯有多种含氧酸,其电离平衡常数如下:
化学式 | HClO4 | HClO3 | HClO2 | HClO |
Ka | 1×1010 | 1×10 | 1×102 | 4×108 |
从物质结构的角度解释以上含氧酸 Ka 依次减小的原因________________________。
(5)钴的一种化合物的晶胞结构如下图所示:
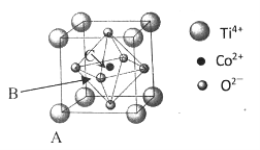
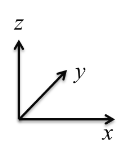
①已知A点的原子坐标参数为(0,0,0),C 点为(1/2,1/2,1/2),则B点的原子坐标参数为___________。
②已知晶胞参数 a = 0.5485 nm,则该晶体的密度为_______________g/cm3。(列出计算表达式即可)